美国批准特朗普接受Regeneron抗体治疗
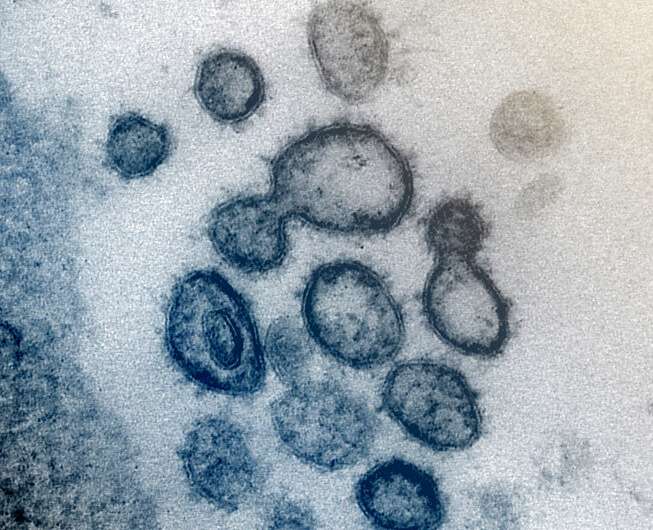
用于治疗唐纳德特朗普总统唐纳德特朗普的Covid-19抗体治疗由美国药物监管机构于周六批准,对于疾病尚未住院但是高风险。
的绿灯对于药物制造商Regeneron来到Regen-Cov2之后,两种实验室制作的组合抗体,显示减少了covid -19相关住院或急诊有潜在疾病的病人。
“批准这些单克隆抗体疗法可以帮助门诊患者避免住院,减轻我们的负担医疗系统,“食品和药物管理局的专员(FDA)斯蒂芬哈恩说。
Regeneron总裁兼首席执行官伦纳德·施莱弗(Leonard Schleifer)补充称,此举是“抗击COVID-19的重要一步高危患者将有机会在感染早期获得有希望的治疗。”
Regeneron的抗体治疗是第二种合成的抗体治疗11月9日,礼来公司开发的一种类似疗法获得了FDA的紧急使用批准(EUA)。
的人类免疫系统自然地发展叫抗体的感染蛋白 - 但由于不是每个人都乘坐足够的反应,像Regeneron和Lilly这样的公司制造了实验室制造的解决方案。
它们的工作原理是与SARS-CoV-2病毒的表面蛋白结合,阻止它入侵人类细胞。
FDA表示,支持Regeneron的EUA的数据来自一项临床试验,试验对象为799名患有轻至中度COVID-19症状的非住院患者。
对于由于各种潜在条件而受到高风险的患者 - 从肥胖到老年到糖尿病 - 住院治疗和急诊室访问,患有静脉治疗的患者的3%发生。
相比之下,接受安慰剂治疗的患者中这一比例为9%。
患者治疗药品与安慰剂上的那些相比,还具有较低的病毒水平。
80000剂
该公司表示,它预计将在11月底之前准备80,000名患者,并在2021年1月底之前达到约300,000名患者。
在美国政府计划的条款下,美国患者可以在美国患者提供。
但随着美国和全球兴奋的情况下,这意味着访问不会普遍存在。仅在过去的两天里增加了超过360,000个新的Covid-19案件。
推荐剂量为每种两种抗体中的1,200毫克,总共2,400毫克,单一输注。
Regeneron已从美国政府获得超过4.5亿美元的4.5亿美元,为其Covid-19在经营经线速度下的药物开发工作。
所谓的单克隆抗体是一种相对较新的药物,被认为很有前途。
上个月,Regeneron对埃博拉病毒开发的抗体药物接受了全FDA批准,即EuA后的下一步。
在COVID-19病例中,Regeneron首先发现了两种对SARS-CoV-2病毒非常有效的抗体,一种来自免疫系统被修饰成类人的老鼠,另一种来自人类。
然后,他们收集产生这些抗体的免疫细胞,并在实验室中培养,以便进行大规模治疗。
像辉瑞和Moderna开发的COVID-19疫苗一样,通过训练免疫系统产生自己的抗体,以便在遇到病毒时做好准备。
©2020 AFP.















用户评论