在癌症发展中,闪耀着基因组的“暗物质”的作用
长RNA分子携带未转化为蛋白质的DNA代码长期以来一直是人类基因组的谜。现在,Duke-Nus医学院的科学家已经找到了一种系统地调查其功能,并发现一些可能在胰腺癌中发挥作用。他们的发现,在期刊上发表了基因组医学,突出了在生物体中研究长期非编码RNA(LNCRNA)的重要性。
RNA长期以来一直被认为是中间体分子;用于RNA的DNA代码,依次蛋白质代码。最近,科学家发现人类中三十亿基对的基因组,只有2%的编码蛋白。剩下的大部分98%的基因组是非编码,并且一旦认为是暗物质人类基因组,没有已知的功能。一些LNCRNA是该基因组暗物质的主要组成部分,已被证明在不同的生物过程中起关键作用,范围从发育到疾病。
“通过结合几个先进的工具,我们能够调查”重要“中的”暗物质“的作用和功能胰癌症,“这项研究的领先作者表示,刘世阳议员是一个MD /博士学位。杜克NUS的学生。
具体来说,研究团队希望识别由称为WNT信号传导的公知途径调节的LNCRNA。该途径调节蛋白质代码的许多基因,但其对LNCRNA的影响尚不清楚。
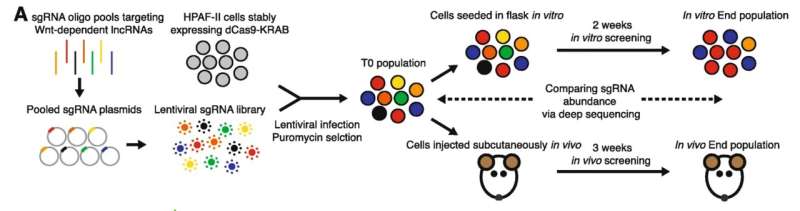
已知WNT信号传导燃料促进一些胰腺癌的生长。关掉这种途径不仅可以帮助治疗胰腺癌,还可以帮助研究人员确定由其调节的基因组的部分。
为此,研究团队转向ETC-159,这是由Duke-Nus和科学,技术和研究机构共同开发的新加坡WNT-抑制药物,目前正在通过临床进展试验作为结直肠癌和妇科癌症子集(卵巢和子宫内膜)的治疗方法。
科学家比较了在胰腺癌和胰腺癌的临床前模型中关闭了LNCRNA时发生的影响力。细胞在实验室培养。他们发现它改变了前者中1,503个Lncrnas的表达,但只改变了后者中的一半的表达。研究人员表示,这突出了在更自然的环境中研究LNCRNA的重要性。
伊斯兰科·彼得雷托副教授,来自杜克 - 努斯的心血管和代谢障碍计划,这项研究的高级协调员解释说:“与以往的研究相比,我们发现了两倍于体内的LNCRNAs的两倍,而不是在体外检测到其中对癌细胞生长仅为体内是重要的,为更有效的癌症治疗提供了重要的线索。“
然后,团队使用基因编辑工具CRISPR来研究在临床前模型和胰腺细胞培养物中关闭1,503个WNT调节的LNCRNA时发生的情况。发现二十一克拉斯能够在生活模型中改变胰腺癌细胞生长,而在癌细胞培养试验中只鉴定了数量的一半。
“我们的研究在基因组的暗物质的主要未知作用中提供了一个独特的窗口,这些作用在功能作用中起着功能作用胰腺癌,并将成为科学界的宝贵资源,研究癌症中受监管的LNCRNA,“Duke-Nus的癌症和干细胞生物学计划主任大卫维修教授,也是该研究的高级协作者。教授Vershup对WNT的开创性研究导致ETC-159的发展。“理解Wnt调节的LNCRNA的子集可以作为癌症中Wnt信号传导的致癌功能的介质提供潜在的精确癌症治疗目标。”
研究小组呼吁进一步研究,以了解这些WNT调节的LNCRNA如何调节癌细胞增殖。
进一步探索













用户评论