新技术聚焦阿尔茨海默病中淀粉样蛋白的神经元摄取
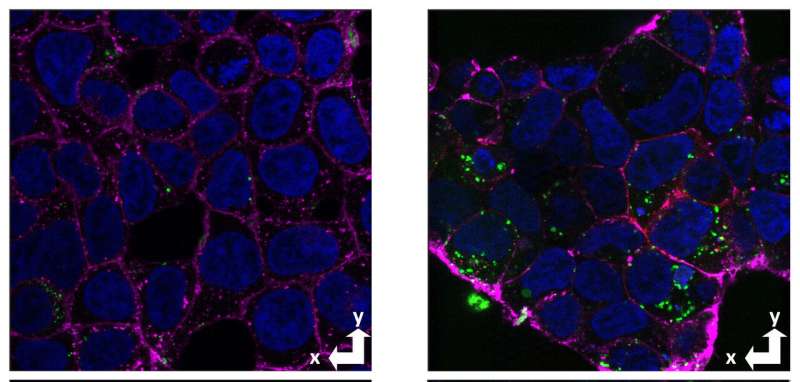
阿尔茨海默病的特征之一是淀粉样斑块的形成——一种叫做淀粉样蛋白的粘性团块,聚集在大脑神经元之间。然而,人们的注意力越来越多地从这些不溶性斑块转向可被神经元吸收并具有高度神经毒性的可溶性β淀粉样蛋白。
加州大学圣克鲁兹分校的研究人员进行了一项新研究,确定了大脑的一部分β淀粉样蛋白蛋白质这被参与神经元摄取有毒肽的受体所识别。研究人员使用了一种新的方法来研究细胞摄取的机制淀粉样蛋白β。他们的研究结果发表在11月2日美国国家科学院院刊,表明针对这一过程可能是阿尔茨海默病药物开发的一种有前途的方法。
“β淀粉样蛋白在细胞内的毒性有很多不同的方式,所以如果我们能阻止神经元摄取它,不是很好吗?”这是我们可以针对的途径,”通讯作者、加州大学圣克鲁兹分校化学和生物化学助理教授耶夫根尼·拉斯卡托夫说。
在这项新研究中,拉斯卡托夫与UCSC化学和生物化学杰出教授格伦·米尔豪瑟(Glenn Millhauser)合作,研究了β淀粉样蛋白与细胞朊病毒蛋白的相互作用。米尔豪瑟的实验室研究朊病毒蛋白的结构和功能,朊病毒蛋白是一种膜蛋白,存在于各种类型的细胞表面,包括大脑中的神经元。
其他研究人员先前的研究表明,正常的细胞朊病毒蛋白(而不是引起朊病毒疾病)与β淀粉样蛋白团块结合,参与摄取和神经毒性。UCSC的研究人员,由研究生Alejandro Foley和博士后研究员Graham Roseman领导,试图测试朊病毒蛋白是否也作为受体,以吸收β淀粉样蛋白的可溶性形式,并确定β淀粉样蛋白中与该受体结合的位点。
研究人员采用了一种基于拉斯卡托夫实验室之前工作的方法,使用β淀粉样蛋白的镜像版本来证明细胞摄取主要是由细胞表面的受体介导的。在早期的研究中,研究人员比较了天然β淀粉样蛋白的摄取和人工合成的β淀粉样蛋白的吸收氨基酸是自然排列的镜像。这种重新排列微妙地改变了蛋白质的结构,从而干扰了它与受体的结合,因此,细胞对镜像版本的吸收大大减少的发现指向了受体介导的吸收。
淀粉样蛋白可以有不同的长度,但毒性最大的变体是42个氨基酸长。为了分离出与受体结合有关的位点,研究人员创建了一个由β淀粉样蛋白的肽段组成的库,例如,仅由1到16或1到30氨基酸组成。对于每个片段,他们分别用天然氨基酸(“L立体异构体”)和镜像氨基酸(“D立体异构体”)制作了一个版本。
在测试了库中所有肽的细胞摄取后,他们发现氨基酸1-30表现出与完整的β淀粉样蛋白相同的立体选择性,L型的摄取要比D型大得多。此外,这部分是完全可溶性的,不形成聚集物,因为它缺少一个长疏水区域,参与淀粉样蛋白聚集成团块和原纤维。
拉斯卡托夫说:“有了这种缩短的β淀粉样蛋白,我们能够将细胞吸收与聚集分离开来,为我们研究吸收提供了一个很好的模型。”
通过评估有和没有朊病毒蛋白的细胞中β淀粉样蛋白的摄取,研究人员首次证明了朊病毒蛋白在可溶性β淀粉样蛋白的细胞摄取中的作用,与它对β淀粉样蛋白的L立体异构体的选择性一致。
非聚集淀粉样蛋白β段1-30显示出同样的朊病毒依赖摄取和立体选择性。研究人员还使用核磁共振波谱来收集有关淀粉样蛋白与细胞朊蛋白结合的相互作用的详细信息。
他们的研究结果表明,β淀粉样蛋白在细胞表面的结合,导致其内化,主要是由于氨基酸序列1-30,而不是聚集状态。当β淀粉样蛋白分子开始聚集时,它们会形成“低聚物”,由少量粘在一起的分子组成,这些分子仍然是可溶性的,可以被神经元吸收。这些可溶性寡聚物被越来越多地认为是触发导致阿尔茨海默病的病理过程的β淀粉样蛋白的形式,但有许多不同的聚集形式。
拉斯卡托夫说:“寡聚物有不同的聚集水平、大小和类型,一个大问题是哪些形式被内化并引起神经毒性。”“我们的研究结果表明,任何形式的氨基酸序列暴露都会与朊病毒蛋白结合。”
米尔豪泽说:“导致阿尔茨海默病的最初步骤可能是朊蛋白介导的可溶性淀粉样蛋白进入神经元,然后在那里聚集,形成有毒的聚集物,最终导致与该疾病相关的特征性斑块。”
虽然朊病毒蛋白质似乎是淀粉样蛋白摄取的主要原因,研究表明其他受体可能提供替代途径。然而,靶向β淀粉样蛋白1-30段或其在受体上结合的位点的药物可能具有治疗阿尔茨海默病的潜力。
米尔豪泽说:“我们的发现为了解阿尔茨海默病开辟了新的途径,并提出了有前途的治疗策略。”
进一步探索












用户评论