Biontech,Pfizer要求欧洲到OK疫苗进行紧急使用
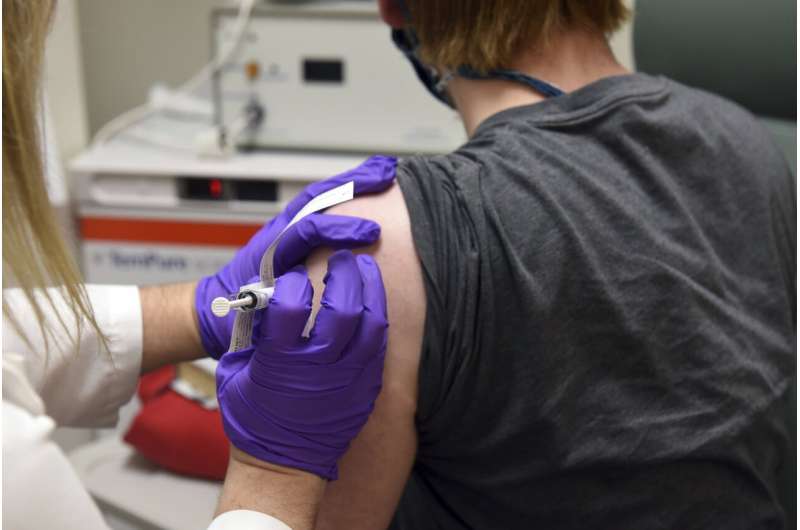
德国制药公司BioNTech及其美国合作伙伴辉瑞公司表示,他们已经向欧洲药品管理局提交了有条件批准其冠状病毒疫苗的申请。
这两家公司周二表示,周一发生的提交完成了他们在10月6日与原子能机构发起的滚动审查流程。
竞争对手现代人表示,这一举动是要求美国和欧洲监管机构允许紧急使用其Covid-19疫苗。
BioNTech表示,如果这种疫苗(目前命名为BNT162b2)获得批准,它可能在2020年底之前开始在欧洲使用。
公司上个月说过临床试验数以万计的参与者表明,疫苗的有效率为95%。的成功率他们说,在特别脆弱的较脆弱的年龄段超过94%。
BioNTech和辉瑞已经向美国食品和药物管理局(fda)和英国监管机构MHRA提交了紧急批准申请,并在澳大利亚、加拿大和日本等其他国家提交了滚动申请。
“自从这次旅程开始以来,患者正在等待,我们已经准备好在潜在授权将允许我们的潜在授权,”辉瑞的首席执行官Albert Bourla在一份声明中表示,我们立即达到Covid-19疫苗剂量。“
德国科学部长周二也说了同样的话安全标准正在批准过程中应用冠状病毒这将是让公众尽可能广泛接受COVID - 19免疫接种的关键。
Anja Karliczek在柏林告诉记者,EMA将于12月11日就BioNTech和辉瑞的批准请求举行公开听证会。
她补充说,疫苗将是自愿的,该当局将努力通知公众在免疫后可能预期的可能副作用,例如头痛,局部疼痛和发烧。
Marylyn ADDO,汉堡的Uke医院医生参与了竞争对手疫苗的试验,表示快速发展疫苗科学家,早期资金和来自以前疫苗的经验的结果是巨大的努力。
©2020相关的压力机。版权所有。未经许可,可能不会发布,广播,重写或重新分配此材料。










用户评论