发现癌细胞如何逃避免疫防御激发新的治疗方法
已知癌细胞用于传播遗传混沌。作为癌细胞分裂,DNA段和甚至整个染色体可以完全复制,突变或丢失。这称为染色体不稳定,纪念斯隆肯特的科学家了解到它与癌症的侵略性有关。从这些染色体中的DNA比特的比特更可能最终将在它们不属于:在细胞的中央核和漂浮在细胞质中的外部的较可能的染色体更可能。
细胞将这些盗窃者DNA解释为病毒侵犯者的证据,从而脱离了它们的内部警报响铃并导致炎症。免疫细胞前往肿瘤部位并搅拌防守化学品。一个神秘的是为什么这种免疫反应被触发癌细胞,不会拼写他们的垮台。
“房间里的大象是,我们并不真正了解癌细胞如何在这种炎症环境中能够生存和茁壮成长,”MSK的医生科学家和人类肿瘤学和发病机构的成员,塞缪尔巴卡努姆说。
根据Bakhoum博士的一项新学习,Bakhoum博士在12月28日发布的日记癌症发现,其原因必须部分地用分子坐在癌细胞的外侧,以在达到邻近之前破坏警告信号免疫细胞。
调查结果有助于解释为什么一些肿瘤没有反应免疫疗法,同样重要的 - 建议将它们敏感到免疫疗法的方法。
检测危险的DNA
警告系统Bakhoum研究博士称为CGAS-Sting。当来自病毒(或不稳定的癌症染色体)的DNA地区的细胞质中的陆地落在细胞的细胞质中时,CGA结合它,形成称为CGAMP的化合物分子,其用作警告信号。在单元格内部,此警告信号激活一个免疫反应称为Sting,它解决了潜在的病毒入侵者的直接问题。
另外,大部分CGAMP还在细胞外行进,在那里它用作相邻免疫细胞的警告信号。它激活它们的刺痛途径,对抗病毒感染的细胞释放免疫发作。
从Bakhoum实验室的以前的工作表明,CGAS-Sting信号传导癌细胞内部导致它们采用免疫细胞的特征 - 特别是爬行和迁移的能力 - 这有助于它们转移的能力。这提供了癌症细胞如何在该过程中存活炎症和辅助转移问题的问题的一部分。新的研究表明,癌细胞如何应对激活CGAS-STING释放到环境中的警告信号。剪刀样蛋白质撕碎信号,提供细胞可以阻止免疫破坏的威胁。
人的三重阴性乳腺癌染色(左)和阳性(右)的实例,用于ENPP1表达。人类三重阴性乳腺癌的抑制负(左)和阳性(右)的eNPP1。
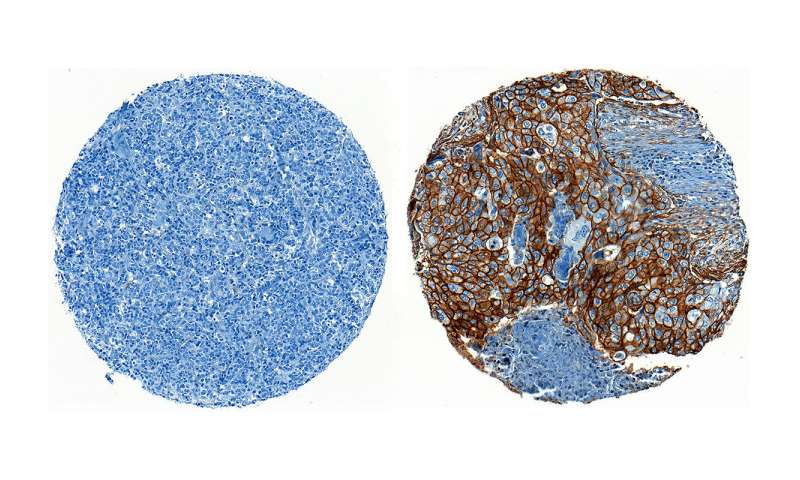
涂层癌细胞的剪刀状蛋白质称为ENPP1。当CGAMP发现其外部的方式时,ENPP1将其缩小并防止信号从达到免疫细胞到达。同时,这种切碎释放称为腺苷的免疫抑制分子,其也会调速炎症。
通过在乳腺癌,肺和结肠直肠癌的小鼠模型中进行的电池,Bakhoum和他的同事博士表明ENPP1就像一个用于免疫抑制和转移的控制开关一样。转向抑制免疫应答并增加转移;关闭它可以免疫应答并减少转移。
科学家们还看着人类癌症样本中的eNPP1。ENPP1表达与增加的转移和抗免疫疗法相关。
赋予免疫疗法权力
从治疗的角度来看,也许研究的最值得注意的发现是翻转ENPP1关闭可以将几种不同癌症类型的敏感性增加到称为检查点抑制剂的免疫疗法药物。研究人员表明,这种方法在小鼠癌症模型中是有效的。
几家公司 - 包括Bakhoum及其同事博士的公司现在正在制定药物以抑制癌细胞上的eNPP1。
Bakhoum博士说,幸运是恩普斯在癌细胞表面上位于癌细胞表面上,因为这使其更容易旨在阻止它的药物。
它也相对具体。由于健康个体中大多数其他组织没有发炎,靶向ENPP1的药物主要影响癌症。
最后,针对eNPP1以两种分开的方式削弱癌症:“你同时增加了外部的CGAMP水平癌症在相邻的免疫细胞中激活刺痛的细胞,同时您还可以防止产生免疫抑制腺苷的产生。所以,你用一块石头击中两只鸟,“巴克努姆博士解释道。
他说,研究的步伐令人难以置信。“如果这项研究结束了帮助患者,我将非常自豪的一件事,因为我们刚刚在2018年开始这项工作。”
他希望在一年内将有eNPP1抑制剂的临床试验。
进一步探索















用户评论