增强免疫治疗有效性的DNA

DNA,最终,它不属于癌症细胞可以更容易引发免疫反应,使肿瘤免疫疗法,UT西南的两项研究的结果显示。结果,今天在线发表癌症细胞表明,提供DNA释放辐射,触发癌细胞对抗癌症免疫治疗可能是一种有效的方法,具有挑战性的治疗。
近十年前,美国食品和药物管理局批准检查点抑制剂、免疫疗法的一种,删除防御使癌症细胞伪装成健康细胞,促使免疫系统攻击他们。2015年,研究人员发现,这些疗法特别承诺引发的癌症细胞的缺陷“错配修复系统校对DNA复制。如果这个系统是错误的,基因突变快速构建,刺激一些细胞变成恶性的。
这些丰富的突变往往使肿瘤难以治疗与传统治疗如化疗和辐射在认为是检查点抑制剂有效反对的原因错配修复缺陷(dMMR)肿瘤。然而,最近的研究表明,只有约一半的dMMR肿瘤患者应对这些疗法,即使nonresponders有相同的丰富的突变,解释了研究负责人Guo-Min Li博士,放射肿瘤学教授和哈罗德·c·西蒙斯的西南大学综合癌症中心。
“一些机制除了这些许多突变必须发挥引发免疫攻击,”李说,他也是Reece a . Overcash Jr .)中心主任研究结肠癌,在UTSW尤金·弗伦克尔博士的荣誉。
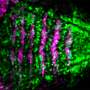
为了更好地理解什么对这些肿瘤引发免疫反应,李和傅杨欣,医学博士博士,病理学教授UTSW和共同通讯作者的研究,转基因人类和小鼠癌细胞移除一种错配修复基因的关键。相对于正常细胞没有操纵,没有一种快速累积在胞质DNA断裂和DNA,或者细胞内液的细胞,而不是在其核DNA通常居住的地方。用辐射治疗这些细胞显著提高多少胞质DNA。
研究人员推断,增加的细胞核内DNA断裂是因过度活跃的基因称为Exo1,工作期间与一种减少错误的DNA复制和修复。进一步的调查显示,当研究人员将这种基因从细胞没有一种或中断蛋白质之间的相互作用所产生的一种Exo1,细胞不再累积DNA断裂和胞质DNA。但是当Exo1仍然活跃在这些细胞,它似乎减少DNA有增无减,促使这个损坏的遗传物质从核泄漏。
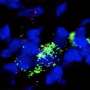
更多的实验表明,这种泄露的DNA激活cGAS-STING通路免疫系统的一部分,感官细胞核外的DNA,并把它解释为一个严重的细胞损伤或感染的迹象。这触发免疫反应。
实际上,当李和他的同事们破坏了这个途径癌症没有一种细胞,肿瘤增长远远快于细胞完整cGAS-STING通路,因为他们免于免疫系统。
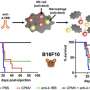
研究人员进一步表明,该DNA传感通道是关键的免疫反应治疗动物携带着一种缺乏肿瘤抑制剂检查站。当这些肿瘤cGAS-STING正常途径,药物是有效的;但是当研究者中断任何途径的一部分,肿瘤拒绝治疗。
本研究与人类患者与dMMR癌症,研究人员测试了肿瘤样品cGAS-STING函数。由于错配修复可以影响任何基因,李解释道,这个途径的基因也经常dMMR肿瘤患者的突变。患者医疗记录显示,高水平的蛋白质表达,或激活,cGAS-STING通路中的更有可能存活癌症不再和/或响应检查点抑制剂比那些较低的蛋白质的表达,表明DNA传感是免疫疗法成功和一个关键免疫反应这些癌症。
李说,这些发现可能最终在未来引导dMMR肿瘤是如何对待。例如,他说,评估肿瘤如何“cGAS-STING通路工作可以帮助医生决定患者将受益于免疫治疗药物,节省他们的时间,金钱,和潜在的副作用。本研究建立在的基础工作下“詹姆斯”Chen博士研究的合著者和西南大学分子生物学教授,他赢得了2019年的生命科学突破奖为他发现注册会计师酶。
研究人员也发现操纵cGAS-STING通路的下游因素的方法,以提高其有效性的肿瘤已经失去了这个DNA传感器,使这些癌症对检查点抑制剂。此外,由于辐射鼓励DNA泄漏到细胞质中,它可以进一步加强这些疗法的有效性。
”这一战略的辐射前免疫疗法在临床试验已经显示成功,但它是如何工作的背后的原因是未知的,”李说。“这两份报告的机制我们报告增加了了解,总有一天会导致完全治疗癌症的新方法。”