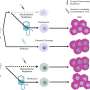
在果蝇体内植入的人类基因揭示了人类发育障碍的细节

迈尔-戈林综合征(Meier-Gorlin syndrome,简称MGS)是一种罕见的遗传发育障碍,会导致侏儒症、小耳朵、小大脑、髌骨缺失和其他骨骼异常。在严重情况下,MGS会导致流产和死产。
Igor Chesnokov博士和他在伯明翰阿拉巴马大学的同事们用一种不寻常的方式研究了这种隐性常染色体疾病——将突变的人类基因植入果蝇体内。具体来说,他们研究了与MGS有关的一种名为Orc6的基因。
一项研究发表在遗传学,作为一篇突出的文章,他们使用了这个动物模型以探测2017年首次报道的一种人类Orc6突变的功能——赖氨酸23到谷氨酸(K23E)的取代。在MGS患者中,K23E突变导致与Chesnokov团队先前研究的Orc6突变类似的可观察到的发育障碍,即酪氨酸225到丝氨酸(Y225S)的取代。
对比这两个突变是很有趣的,因为23号位置靠近前端,或n端结构域,是折叠形成Orc6蛋白的长链连接氨基酸。225位靠近Orc6蛋白链的末端或c端结构域。
Orc6是起源识别复合体(ORC)的一部分。这种蛋白质复合物对于启动细胞中的DNA复制至关重要,无论是酵母、果蝇、人类还是任何其他真核生物。没有DNA分裂,细胞就不能分裂,有机体就不能生长。如MGS所示,糟糕的划分将阻碍增长。
在之前发表在《美国医学遗传学杂志》上的关于Y225S突变的研究中,UAB的研究人员发现,Orc6的c端结构域对于蛋白质-蛋白质相互作用非常重要,有助于构建ORC复合体。在目前的研究中,Chesnokov和同事们发现Orc6蛋白n端结构域的K23E突变破坏了蛋白质与DNA结合的能力。这种特定的绑定是ORC函数中的重要步骤。
因此,虽然这两种突变有不同的基础分子机制,它们都导致复制前复合物形成缺陷和DNA复制减少,并且它们在MGS患者中产生类似的表型。
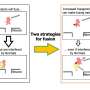
这项研究的关键之一是创造部分人类基因和部分果蝇基因的Orc6嵌合基因。这就是为什么这是必要的。将人类Orc6基因植入果蝇体内,并不能防止Orc6基因缺失对果蝇的致命影响;换句话说,完整的人类Orc6不能取代果蝇Orc6的功能,这是由于Orc6与两种生物中ORC核心相互作用的差异。
然而,当UAB的研究人员制造了一种n端结构域为人类、c端结构域为果蝇的杂交Orc6时,杂交Orc6能够完全拯救果蝇,并且它们长成了与果蝇无法区分的成年果蝇水果携带野生型Orc6的果蝇。这种杂交Orc6可以用来检测K23E突变果蝇并研究其分子机理。
切斯诺科夫说:“这种混合方法可以研究人类蛋白质在动物系统中的功能,它揭示了Orc6蛋白进化保守和可变结构域的重要性。”我们相信这种混合方法不仅为研究新Orc6开辟了广阔的道路突变用于医学和一般科学目的,但也可能用于其他人性化模型。”
总之,切斯诺科夫教授说,这种人化果蝇模型具有独特的优势,能够区别测试果蝇、人类和嵌合Orc6蛋白,以揭示蛋白质的保守性和差异性特征及其在后生动物细胞中的功能。
更多信息:Maxim Balasov等人,Meier-Gorlin综合征的人性化果蝇模型揭示了Orc6蛋白的保守和发散特征,遗传学(2020)。DOI: 10.1534 / genetics.120.303698