新的人性化小鼠模型提供了有关免疫疗法抗性的洞察力

维斯塔尔研究所(Wistar Institute)的科学家创建了一个先进的人源化免疫系统小鼠模型,使他们能够检查黑色素瘤中对免疫检查点阻滞疗法的抗性。它揭示了肥大细胞的核心作用。这些发现今天发表在《杂志》上自然通讯。
检查点抑制剂彻底改变了晚期黑色素瘤的治疗选择。然而,由于耐药性病变的重新出现,只有一小部分患者对这种治疗作出反应和一些复发。
Wistar Institute Centute Center的成员Rajasekharan Somasundaram博士Rajasekharan Somasundaram博士说:“为了更好地理解为什么有些癌症不反应或对检查点疗法具有抵抗力,我们需要更模仿人类肿瘤免疫环境的更临床前模型。”谁是本文的第一作者。
由于鼠和人类免疫系统的临界差异,小鼠模型不允许研究人类独特的免疫机制。“人性化”小鼠模型被广泛用于模仿小鼠的人类免疫系统。
韦斯塔尔的新人道化鼠标模型依靠移植人类干细胞以及经过独特设计的组织,以产生人类细胞因子的组合,从而产生更相关的模型系统,用于评估新的免疫肿瘤疗法和针对针对性的有效治疗方法肿瘤微环境。
“我们的新型人性化小鼠模型具有更长的寿命,并使我们能够研究人类肿瘤移植后免疫疗法的治疗反应,”索马桑达拉姆(SomasundaramWistar研究所癌症中心,Wistar Institute Helanoma研究中心主任,研究的共同培训。
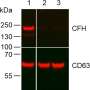
研究人员将人类转移性黑色素瘤细胞系移植到其人源性小鼠模型中,并用抗PD-1抗体疗法治疗它们。通过研究免疫细胞浸润到肿瘤中,Somasundaram及其同事观察到抗PD-1处理的肿瘤中有大量浸润的肥大细胞。肥大细胞是整个身体中发现的免疫细胞,尤其是在皮肤和粘膜中,它们是针对病原体的第一道防线。在接受免疫检查点疗法的黑色素瘤患者的样品中,该小组在非反应性肿瘤中看到了较高的肥大细胞。
作者表明,与接受任何一种治疗的小鼠相比,将抗PD-1治疗与能够耗尽肥大细胞的小分子抑制剂结合导致肿瘤的完全消退,并长期生存。重要的是,在停止治疗并发展了针对黑色素瘤肿瘤的记忆T细胞反应后,在四个星期后没有显示出任何复发的迹象。
“我们的结果表明桅杆细胞与抗PD-1疗法的耐药性有关,并且耗尽肥大细胞有益于免疫检查点治疗赫林说。小分子抑制剂用于治疗黑色素瘤患者。”
进一步探索












用户评论