一种帮助免疫系统反击癌症的新方法
威斯康星大学医学与公共卫生学院的科学家正在破坏新的基础,以使癌细胞更容易受到人体自身的免疫系统的攻击。
在小鼠中工作,放射学教授Jamey Weichert和人类肿瘤学教授Zachary Morris在其方法中使用了两种不同的技术,使用靶向放射性核球,将两种不同的技术结合在一起治疗,该,专门为低剂量的细胞射辐射提供癌细胞,然后进行免疫疗法,这有助于免疫系统认识并摧毁癌症细胞。这动物研究正在为未来的人类和兽医临床试验奠定基础。
Weichert解释说:“这具有巨大的优势,因为我们可以系统地靶向肿瘤,无论数量和解剖位置如何。”“我经常将其描述为用这种较低的辐射擦拭肿瘤,以使免疫系统更容易识别它。”
该团队已从国家癌症研究所获得了1,250万美元的资金,以进一步开发这种方法来治疗各种癌症,包括前列腺癌和狗的癌症。
研究工作包括由Weichert,Morris和其他UW -Madison研究人员组成的四个项目和四个研究和支持核心,这是威斯康星大学Carbone Cancer Center的许多成员。
与传统的外部梁辐射疗法相反,该疗法以非靶向的方式递送到身体的所有或大部分,靶向放射性核素疗法涉及将放射性原子(也称为放射性核素)连接到主要被吸收的分子由肿瘤细胞。
Weichert的团队使用了一个放射性元素和一个分子,该分子模仿了一种在快速分裂的癌细胞中发现的脂质。他们还使用成像技术来实现注射到血液中的药物的精确剂量。
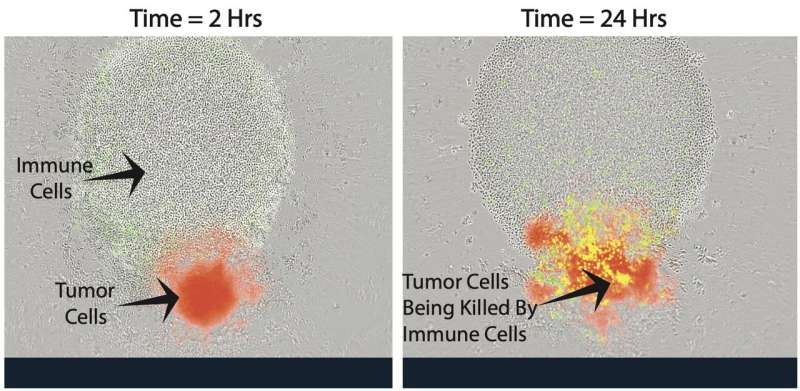
科学家在小鼠中发现,使用免疫疗法与靶向放射性核素疗法结合使用比单独的方法更强大。他们将进一步研究不同免疫疗法剂的组合,以抵抗癌症逃避免疫系统的许多方式。
例如,某些癌细胞具有一种试图攻击它们的“关闭”免疫细胞的方法。该团队使用免疫检查点抑制剂,这些抑制剂是阻断癌细胞中和免疫细胞能力的药物,因此免疫细胞具有战斗机会。
另一个研究领域的重点是如何激活免疫细胞本身。儿科和人类肿瘤学教授Paul Sondel正在研究一bob电竞种“原位疫苗”,可吸引免疫细胞到肿瘤中并激活它们,以便它们在肿瘤部位识别和杀死癌细胞。该技术训练免疫系统,以类似于针对传染病的疫苗的方式保留特定癌症的记忆,该疫苗将免疫系统指导识别细菌和病毒等病原体。
医学教授道格拉斯·麦克尼尔(Douglas McNeel)通过将其团队在前列腺肿瘤疫苗与靶向放射性核素治疗相结合,将这种协同方法应用于前列腺癌。他的团队将调查靶向放射治疗是否首先会削弱肿瘤,从而导致受刺激的免疫细胞攻击的疫苗性能更好前列腺癌细胞。
莫里斯将这些组合疗法比作破坏肿瘤的推土机。
推土机的点火需要打开,在某些情况下,癌症疫苗可以促进这一过程。推土机的动力和加速需要燃料,这可以通过扩展和增殖的癌症攻击免疫细胞的药物提供。检查点抑制剂可以通过脱离免疫系统的制动器来进一步加速加速。当有多个肿瘤时,靶向放射性核素疗法可以通过血液传播到体内的每个肿瘤。这铺平了抗抗的路径瘤免疫反应会杀死整个人体的癌细胞。
该小组研究了迄今为止的一组狭窄的有针对性的放射性核素疗法和免疫疗法,这是UW2020赠款从UW -Madison办事处的研究和研究生教育副教育和威斯康星州校友研究基金会的主要工作。国家癌症研究所的资金将使他们扩大工作,以包括多种类型的疗法,并孤立地研究它们。
莫里斯说:“这里的变量数量开始变得巨大,并且突出显示了我们对如何优化这些疗法之间相互作用的了解,”莫里斯说。“真正理解这些的唯一方法是以一种非常受控的方式进行实验进行正面比较,就像这笔赠款为我们提供了资源。”
参与该组的其他人是数据分析,放射药,治疗剂的产生以及当业主同意尝试实验治疗时,这些治疗方法在犬科学患者中的应用。其中包括Kyungmann Kim,Michael Newton,Bryan Bednarz,Joe Grudzinski,Reinier Hernandez,Jonathan Engle和David Vail。
Weichert说:“该国实际上只有其他一个或两个机构可以进行此类研究,可以使用必要的专业知识和资源。”“在这些学科中,我们都拥有世界上最高的人。我们相信我们正在这里推出一个新的癌症治疗领域。这非常令人兴奋,研究团队令人难以置信。”
进一步探索