“芯片的器官”系统揭示了人类消化道中的细菌如何影响神经系统疾病

在很多方面,我们的大脑和我们的消化道是紧密相连的。感到紧张可能会导致胃部疼痛,而来自肠道的饥饿信号会让我们感到烦躁。最近的研究甚至表明,生活在我们肠道中的细菌可以影响一些神经系统疾病。
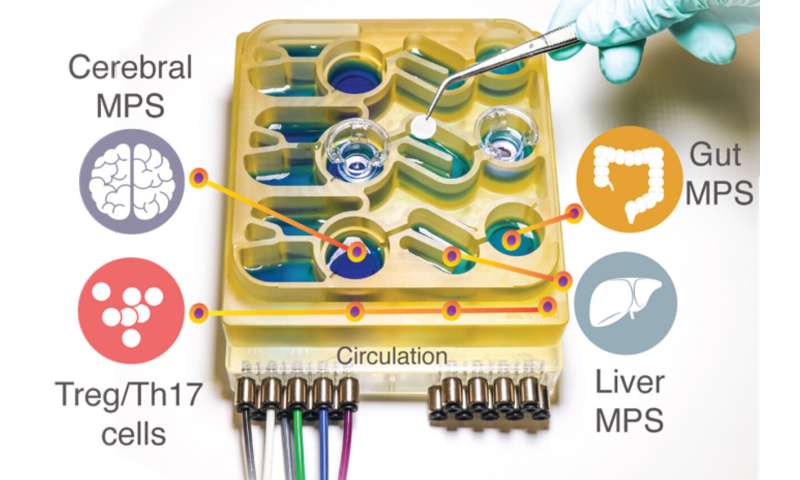
在动物(如老鼠)中建立这些复杂的相互作用的模型是困难的,因为它们的生理机能与人类非常不同。为了帮助研究人员更好地理解肠道-大脑轴,麻省理工学院的研究人员开发了一种“器官芯片”系统,可以复制大脑、肝脏和结肠之间的相互作用。
使用该系统,研究人员能够模型肠道微生物对健康的脑组织和组织样本来自帕金森病的患者。他们发现,通过肠道中的微生物产生并将其运输到大脑的短链脂肪酸可对健康和患病的脑具有非常不同的影响细胞。
“虽然短链脂肪酸在很大程度上对人类健康有益,但我们观察到,在某些条件下,它们会进一步加剧某些大脑病理,如与帕金森病相关的蛋白质错误折叠和神经元死亡,”麻省理工学院博士后、该研究的主要作者马丁·特拉普卡尔(Martin Trapecar)说。
Linda Griffith,教学创新工程学院教授,生物工程和机械工程教授,Rudolf Jaenisch,麻省理工学院生物学教授,麻省理工学院怀特黑德医学研究所成员,是这篇论文的资深作者bob88体育平台登录科学推进。
肠脑连接
几年来,格里菲斯的实验室一直在开发微生理系统——一种小型设备,可以用来培养由微流体通道连接的不同器官的工程组织模型。Griffith说,在某些情况下,这些模型可以提供比动物模型更准确的人类疾病信息。
在去年发表的一篇论文中,Griffith和Trapecar使用一个微生理系统来模拟肝脏和结肠之间的相互作用。在这项研究中,他们发现肠道微生物产生的分子短链脂肪酸(SCFAs)在特定条件下会恶化与溃疡性结肠炎相关的自身免疫性炎症。短链脂肪酸,包括丁酸,丙酸和醋酸盐,也对组织有好处,包括增加免疫耐受,他们占我们从食物中获得的能量的约10%。
在这项新的研究中,麻省理工学院的研究小组决定加入大脑和循环免疫细胞他们的多器官系统。大脑与消化道有许多相互作用,可以通过肠道神经系统或通过免疫细胞、营养物质和器官之间的激素循环发生。
几年前,CALTECH的微生物学教授Sarkis Mazmanian发现了SCFA和帕金森病在小鼠中的联系。他表明SCFA是由细菌产生的,因为它们在肠道中消耗未消化的纤维,加快了疾病的进展,而无菌环境中提出的小鼠越来越慢。
Griffith和Trapecar决定利用他们的微生理模型进一步探索Mazmanian的发现。为了做到这一点,他们与Jaenisch在Whitehead研究所的实验室合作。Jaenisch之前开发了一种将成纤维细胞从帕金森患者转化为多能干细胞这些细胞可以被诱导分化成不同类型的脑细胞——神经元、星形胶质细胞和小胶质细胞。
超过80%的帕金森氏症病例不能与特定的基因突变有关,但其余的确实有遗传原因。麻省理工学院的研究人员用于帕金森氏症模型的细胞携带有一种突变,这种突变会导致一种叫做阿尔法突触核蛋白的蛋白质的积累,这种蛋白质会损害神经元并导致脑细胞炎症。Jaenisch的实验室还培育了一些脑细胞,这些脑细胞矫正了这种突变,但在其他方面与患病细胞在基因上是相同的,而且来自同一个病人。
Griffith和Trapecar首先在没有连接到任何其他组织的微生物学系统中研究了这两套脑细胞,发现帕金森的细胞显示出比健康的矫正细胞更多的炎症。帕金森的细胞也有损害,他们可以弥合脂质和胆固醇的能力。
相反的效果
然后,研究人员将脑细胞与结肠和肝脏的组织模型连接起来,利用通道让免疫细胞和营养物质(包括SCFAs)在它们之间流动。他们发现,对于健康的脑细胞来说,暴露在短链脂肪酸中是有益的,有助于它们成熟。然而,当大脑从帕金森氏症患者身上提取的细胞暴露在短链脂肪酸中,有益作用就消失了。相反,这些细胞经历了更高水平的蛋白质错误折叠和细胞死亡。
即使从系统中除去免疫细胞,导致研究人员也会发现这些效果是假设通过对脂质代谢的变化介导的影响。
“短链脂肪酸似乎可以通过影响脂质代谢而与神经退行性疾病有关,而不是直接影响特定的免疫细胞群,”特拉普卡说。“现在我们的目标是试图理解这一点。”
研究人员还计划建立其他类型的模型神经系统疾病这可能会受到肠道微生物群的影响。格里菲斯说,这些发现支持了人类组织模型可以产生动物模型不能产生的信息的观点。她现在正在研究一个新版本的模型,其中将包括连接不同组织类型的微血管,使研究人员能够研究组织间的血液流动如何影响它们。
格里菲斯说:“我们应该真正推动这些技术的发展,因为在我们的模型中引入更多的人类特征是很重要的。”“我们已经能够开始深入了解人类的状况,而这很难从老鼠身上得到。”
进一步探索










用户评论