胃特异性c-Myc过表达与胃癌
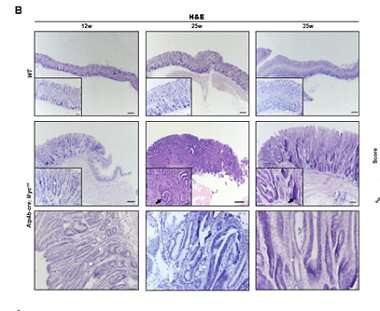
胃癌是世界上最常见的恶性癌症之一。由于早期胃癌的阶段通常持续较长时间,且缺乏明显的症状,因此早期胃癌的诊断非常困难。因此,胃癌患者通常预后差,生存率低。在胃癌的进展过程中,遗传因素起着不可缺少的作用。c-Myc是一种致癌基因,在包括胃癌在内的多种肿瘤中异常高表达。例如,高表达c-Myc的Hi-Myc小鼠模型已广泛应用于前列腺癌的研究。然而,目前还没有c-Myc表达增加的胃癌小鼠模型,也不清楚c-Myc在早期是如何促进胃癌的。
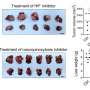
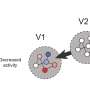
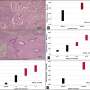
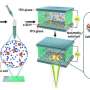
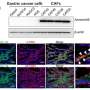
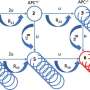
在发表在《波斯尼亚基础医学杂志》,作者成功生成了胃特异性c-Myc转基因小鼠模型。他们发现在Atp4b+胃壁细胞中过表达c-Myc可诱导小鼠胃腺瘤。机制上,c-Myc通过AKT/mTOR通路促进肿瘤发生。AKT抑制剂(MK-2206)或mTOR抑制剂(雷帕霉素)可抑制c-Myc过表达胃癌细胞的增殖和c-Myc转基因小鼠的胃癌发生。
总体而言,本研究作者首先建立了胃特异性c-Myc转基因小鼠模型,为后续胃癌研究提供了全新的动物模型。此外,他们的研究结果强调,c-Myc过表达诱导胃肿瘤的发生是通过激活AKT/mTOR通路。
更重要的是,他们的研究对早期肿瘤的诊断和分子靶向治疗具有重要的临床意义胃癌.
进一步探索
更多信息:Jing Liu等。胃特异性c-Myc过表达通过AKT/mTOR信号通路驱动小鼠胃腺瘤,《波斯尼亚基础医学杂志》(2020)。DOI: 10.17305 / bjbms.2020.4978
所提供的波黑联邦基础医学协会
引用:胃特异性c-Myc过表达与胃癌(2021,1月22日)检索自2022年6月10日//www.pyrotek-europe.com/news/2021-01-stomach-specific-c-myc-overexpression-gastric-cancer.html
本文件受版权保护。除用于个人学习或研究的公平交易外,未经书面许可,不得转载任何部分。内容仅供参考之用。