获取ZIF的负载!更好地提供癌症免疫治疗
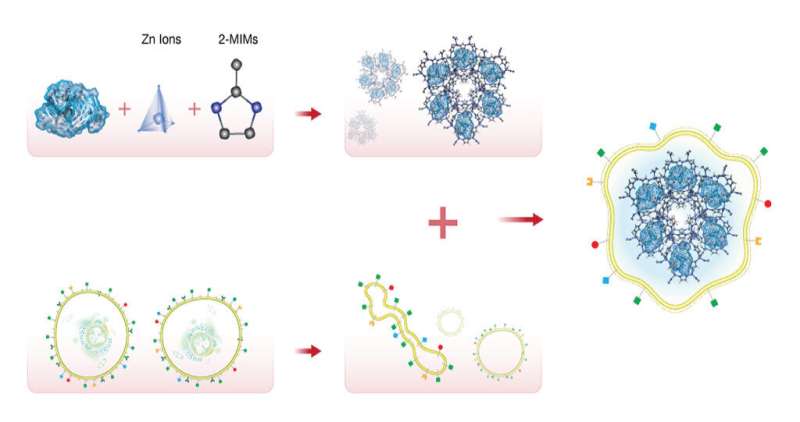
负载在多孔金属有机框架上的抗体被肿瘤周围的酸性环境释放出来,避免了单独管理抗体的不良影响。
加载癌症免疫治疗药物在金属上有机框架改善了交付以及治疗白血病的缓释药物。此外,用癌细胞膜包裹载药框架改善了对实体肿瘤的靶向传递。这些发现可能会导致更安全、更可靠的癌症免疫疗法。
KAUST化学家Niveen Khashab说:“我们相信我们的发现非常重要,因为它们表明,免疫疗法的不良副作用可以通过选择正确的传递载体来调节。”“他们还表明,通过适当的表面功能化,可以实现靶向传递。”
癌症免疫疗法包括使用药物来调节免疫系统让它更有效地攻击肿瘤。Nivolumab就是这样一种药物,它可以抵消一种癌症免疫逃避策略,该策略涉及表达使T细胞失活的PD-L1分子细胞通过阻断PD-1分子的表面
然而,像其他“免疫检查点抑制剂”一样,nivolumab会导致免疫相关的不良反应,其中过度的T细胞激活会导致针对受体器官的免疫反应。科学家们正在寻找改善nivolumab等抗体释放的方法,使其释放缓慢、持续和有针对性,不良影响最小。
Khashab的小组研究了一种称为沸石咪唑酸盐(ZIF-8)的金属有机框架,这是一种由锌离子亚基附着在有机甲基咪唑上形成的结晶固体。Khashab小组的博士生Somayah Qutub说:“在过去几年里,ZIF-8纳米颗粒在癌症药物输送方面显示出了巨大的潜力。”“它们是由锌离子和咪唑组成的,它们是人体内天然存在的。”这使得zif -8的生物相容性、可生物降解性和高多孔性成为安全装载和输送nivolumab等药物的理想选择。
Khashab的团队将nivolumab加载到ZIF-8上,并测试其对白血病细胞的影响。他们发现,当接近微酸性肿瘤微环境时,抗体会缓慢地从ZIF-8框架中释放出来。这一过程可以防止T细胞被癌细胞灭活,从而可以攻击白血病细胞。
研究小组还测试了将抗体传递给的系统实体肿瘤无论是在培养皿实验中还是在老鼠身上。他们将装载nivolumab的ZIF-8与被靶向的癌细胞的膜包裹起来。这导致该系统精确地传递到肿瘤,随后缓慢和持续的药物释放。重要的是,小鼠表现出微不足道的毒性药物,显著抑制了肿瘤生长和延长生存期。
“我们的下一步是改进这个系统,”Qutub说。“我们正在将免疫治疗药物与其他抗癌方法结合起来,以产生协同效应。我们还在努力用其他材料优化我们的癌细胞膜涂层,这样系统就可以很容易地重现、扩展并与生物制药行业标准兼容。”
进一步探索











用户评论