研究发现大脑的“接线绝缘”是与年龄有关的大脑恶化的主要因素
朴茨茅斯大学领导的一项新研究确定,与年龄相关的大脑恶化的主要因素之一是失去了一种称为髓磷脂的物质。
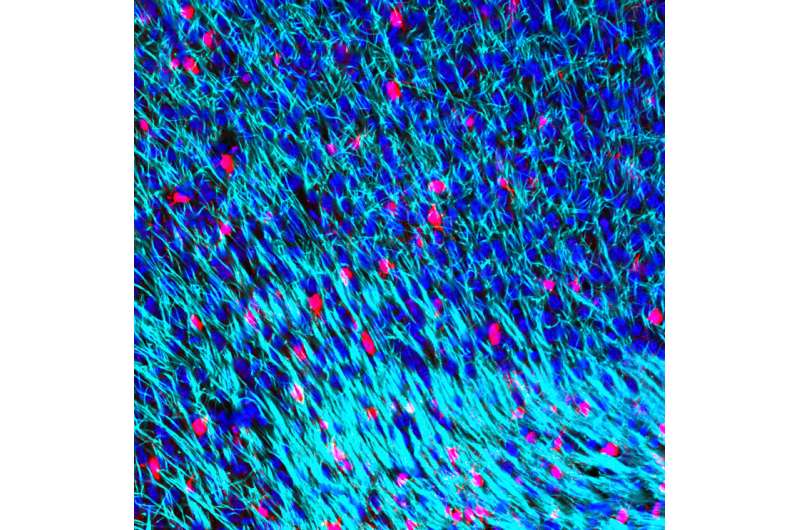
髓磷脂像保护性和绝缘塑料外壳一样,在脑- 称为轴突。髓鞘对于超快速交流至关重要神经细胞那在人脑的超级计算机力量背后。
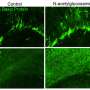
损失髓线结果导致认知能力下降,并且是多种神经退行性疾病的核心,例如多发性硬化症和阿尔茨海默氏病。这项新研究发现细胞随着年龄的增长,这种驱动髓磷脂修复效率降低,并确定了受衰老影响最大的关键基因,从而降低了细胞替代损失髓磷脂的能力。
这项研究于本周发表在《期刊》上衰老细胞,是朴次茅斯大学教授与德国杜塞尔多夫大学的Kasum Azim博士领导的国际合作的一部分,以及米兰的玛丽亚·皮亚·阿布布拉西奥(Maria Pia Abbracchio)教授和帕多瓦(Padua)的安德里亚·里维拉(Andrea Rivera)博士。
巴特教授说:“每个人都熟悉大脑的灰质,但很少有人知道白质,其中包括连接大脑所有不同部位的绝缘电线。
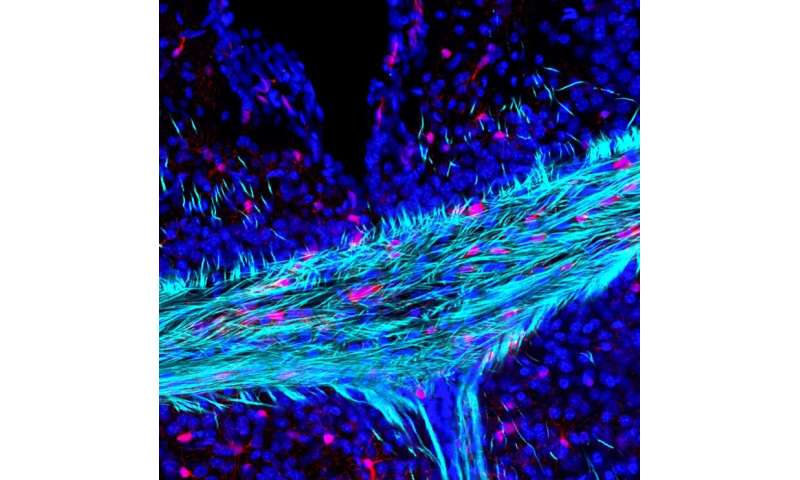
“衰老大脑的一个关键特征是逐渐丧失白质和髓磷脂,但是这些过程的原因很大程度上是未知的。产生髓鞘的脑细胞(称为少突胶质细胞)所需的少量细胞被称为少突胶质前体的干细胞代替。衰老的大脑。”
这项研究的首席作者里维拉博士在朴茨茅斯大学,现在是帕多亚大学的研究员,他解释说:“通过将年轻老鼠大脑的基因组与老鼠的基因组进行比较,我们确定了哪个过程受到衰老的影响。这些非常复杂的分析使我们能够揭示少突胶质细胞补充及其产生的髓磷脂的原因。
“我们确定了与这些特定前体相关的基因GPR17,是衰老大脑中受影响最大的基因,GPR17的丧失与这些前体积极作用以替代丢失的髓磷脂的能力降低。”
这项工作仍然非常持续,为如何诱导少突胶质细胞前体细胞“复兴”的新研究铺平了道路,以有效地补充失去的白质。
杜塞尔多夫大学的阿齐姆博士说:“这种方法有望靶向衰老的大脑和脱髓鞘疾病的髓鞘丧失,包括多发性硬化症,阿尔茨海默氏病和神经精神疾病。的确,我们只触及了冰山和未来的冰山和未来的小费我们研究小组的调查旨在将我们的发现带入人类的翻译环境中。”
里维拉(Rivera)博士在朴茨茅斯大学(University of Portsmouth)进行了本研究中发表的关键实验,他被授予享有声望的MSCA卓越印章@UNIPD奖学金,以翻译这些发现,并与Raffele de De De Cromant在人类大脑中进行进一步调查。帕多瓦大学人类解剖研究所的Caro,Andrea Porzionato和Veronica Macchi。
这项研究由BBSRC和MRC向Butt教授提供资金,以及英国和意大利MS社会(分别为Butt和Abbracchio教授),以及瑞士国家资金奖学金和德国研究委员会(Azim博士)。安德里亚·里维拉(Andrea Rivera)博士得到了解剖学会博士的支持。学生资格(与Butt教授)和卓越的MSCA @Unipd(Rivera博士)。
MS Society研究助理主任Emma Gray博士说:“ MS可能是无情和痛苦的,可悲的是,仍然没有治疗方法可以停止残疾进展。我们可以看到一个未来,没有人必须担心MS获得MS更糟糕的是,但是要实现这一目标,我们需要找到修复受损的髓磷脂的方法。这项研究阐明了为什么随着年龄的增长,驱动髓磷脂修复的细胞会变得不那么高效,我们为能够提供资金而感到自豪。我们对衰老的脑干细胞的理解为我们提供了一个新的目标,可以帮助减慢MS的发展,并可能对未来的治疗产生重要影响。”
进一步探索