蛋白质组学分析识别侵袭性人类癌症的潜在药物靶标
 Monsivais, et al/Oncogene, 2021" width="768" height="406">
Monsivais, et al/Oncogene, 2021" width="768" height="406">
贝勒医学院的研究人员表明,蛋白质组学或所有蛋白质数据的分析来自侵略性人类癌症是识别潜在的新型治疗靶标的有用方法。他们在期刊上报告oncogene.,鉴定与研究的七种癌症类型中的每种侵蚀性疾病的临床测量相关的“蛋白质组学签名”。在不同类型的癌症之间共享一些签名,包括改变代谢的细胞途径。重要的是,实验结果提供了概念证明,其蛋白质组学分析方法是识别潜在治疗目标的有价值的策略。
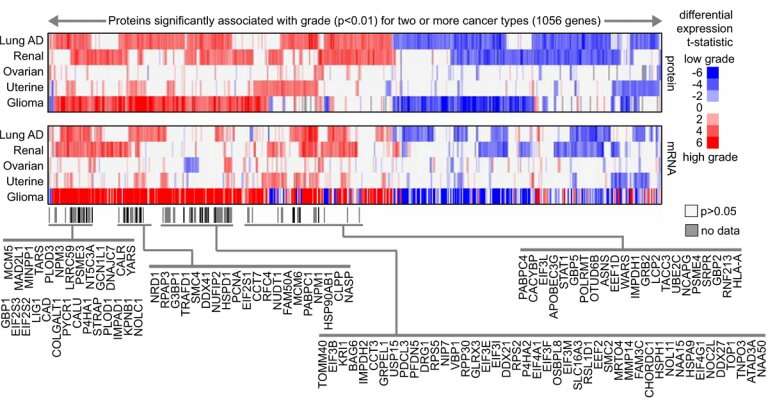
“这项研究有两个值得注意的方面。一个是我们探索了蛋白质组学景观癌症寻找与攻击性癌症相关的癌症相关的蛋白质,“贝勒的Dan L Duncan综合癌症中心癌症生物信息学教授Chad Creighton博士Chad Creighton博士表示。”我们分析了蛋白质包括大约800个肿瘤的数万个蛋白质的数据,包括七种不同癌症类型临床蛋白质组学肿瘤分析联盟(CPTAC)基于质谱的蛋白质组数据集提供了乳腺、结肠、肺、肾、卵巢、子宫和儿童胶质瘤。”
对CPTAC数据集的计算分析确定了与侵袭性癌症相关的蛋白质组学特征。这些信号表明,改变的细胞途径可能会推动侵略性癌症行为,并可能代表新的治疗靶点。每一种癌症都有其独特的蛋白质组学特征签名为了它的侵略性形式。有趣的是,某些签名对不同类型的癌症是常见的。
本研究的另一方面是提供概念证明,蛋白质组学分析是识别可能被操纵以控制癌症生长的侵袭性疾病驱动程序的有用策略。
“这正是我们能够与这个新的,非常强大的数据集做些什么,”贝勒的病理学和免疫学助理教授Diana Monsivais博士说。“我们专注于子宫癌数据,其中计算分析鉴定了与侵略性癌症相关的许多蛋白质中的改变。我们选择了蛋白激酶,将为治疗剂的更强大候选人来说,酶。“
在数百个最初的候选基因中,研究人员选择了四种激酶用于子宫癌细胞系的功能研究。他们发现,激酶不仅在子宫癌细胞系中表达,而且操纵一些激酶的表达降低了一些子宫癌细胞的存活或迁移能力。细胞迁移是癌细胞的一种特性,它允许癌细胞扩散到其他组织。
这项工作是两个贝勒中心的成果合作,丹邓肯综合癌症中心和药物发现中心。
“乍得对新的CPTAC数据集进行了这个令人讨厌的分析,并有兴趣在人类癌症中验证它。他对我们进行了执行功能研究以确定一些蛋白质是否可以转化为新肿瘤癌的新靶标,”Monsivais说。“我们的实验提供了蛋白质组学的概念证明分析是一个有用的策略,不仅要更好地了解驱动癌症的癌症,而是确定控制它或消除它的新方法。“
从历史上看,研究人员一直只生成转录组数据(信使RNA (mRNA)可以翻译成蛋白质)。观察CPTAC提供的蛋白质数据本身,使研究人员能够从这些癌症中提取新的一层信息,”Creighton说。“在这项研究中,我们比较了mRNA和蛋白质的签名,尽管在很多情况下它们重叠,但大约有一半的蛋白质蛋白质组学对应的mRNA签名中没有包含签名,表明需要同时包含mRNA和蛋白质癌症研究中的数据。“
进一步探索











用户评论