克罗恩病可能是由免疫信号失败引起的

克罗恩病患者通常会使用强效抗炎药物进行治疗,这种药物不仅作用于消化道,而且作用于全身,可能会产生意想不到的、通常很严重的副作用。佛罗里达州斯克里普斯研究所的马克·桑德德鲁德博士的实验室的一项新研究表明,一种更有针对性的治疗方法是可能的。
克罗恩病起源于慢性炎症在消化道,通常是小肠。在美国,有超过50万人患有这种疾病,这种疾病会使人衰弱,需要反复手术来切除不可逆转的损伤肠组织。
写在杂志上自然4月7日,Sundrud的团队发现某些免疫细胞在小肠中已经进化出一种分子感应机制来保护自己免受高浓度胆汁酸的毒性作用。他们发现,这种感觉机制可以用小型药物样分子来操纵,这种治疗减少了小鼠的小肠炎症。
“似乎这些被称为T效应细胞的免疫细胞已经学会了如何保护自己不受胆汁酸的伤害,”Sundrud说。“这些T细胞利用整个基因网络与小肠内的胆汁酸安全地相互作用。至少在一些克罗恩病患者中,这一通路可能发生故障。”
胆汁酸在肝脏中产生,并在进食时释放出来,帮助脂肪和脂溶性维生素的消化和吸收。它们在小肠末端一个叫做回肠的区域被主动地重新捕获,在那里它们穿过包含肠道免疫细胞密集网络的组织层,最终重新进入血液返回肝脏。
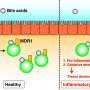
由于胆汁酸是洗涤剂,如果系统变得不平衡,胆汁酸会引起毒性和炎症。多亏了一个复杂的信号系统,整个过程一直嗡嗡作响。肝细胞和肠屏障细胞中的受体都能感觉到胆汁酸的存在,如果胆汁酸过多,它们就会告诉肝脏减少胆汁酸的分泌,如果胆汁酸不足以消化一顿牛排,它们就会分泌更多的胆汁酸。
考虑到胆汁酸对细胞的潜在破坏,科学家们想知道那些生活在或访问小肠的免疫细胞是如何忍受胆汁酸的存在的。Sundrud的团队此前曾报道,当一种重要的免疫细胞子集CD4在血液中循环时,一种名为MDR1的基因,也被称为ABCB1,就会被激活+T细胞进入小肠。MDR1作用于暂时性T细胞,抑制胆汁酸毒性和小肠炎症。
在这项新的研究中,Sundrud的团队使用了一种先进的基因筛选方法来揭示T细胞是如何在小肠中感知和响应胆汁酸来增加MDR1活性的。
“T细胞花费大量时间和精力来预防胆汁酸引起的压力和炎症的基本发现,突出了我们如何看待和治疗克罗恩病的全新概念,”Sundrud说。“这就像我们一直在错误的地点挖掘宝藏,而这项工作给了我们一张新的地图,显示了X标记的地点。”
T细胞在其细胞核中含有一种被称为CAR的受体分子,简称为组成性雄烷受体。在小舞台上表演肠研究小组发现,CAR可以促进MDR1的表达,并在激活一种重要的抗炎基因IL-10中发挥作用。
“当我们用激活CAR的药物样小分子治疗小鼠时,结果是局部解毒胆汁酸和减少炎症,”Sundrud说。
孙德德说,探索CAR激活的治疗潜力需要谨慎和创造性,因为CAR对分解和清除肝脏中的其他物质也很关键,包括许多药物。
“最终,从这项工作中产生的克罗恩病治疗可能会在小肠T细胞局部激活CAR,或者瞄准另一个基因,这个基因同样负责促进小肠T细胞和胆汁酸”,Sundrud说。
同样有趣的是,研究小组发现,胆汁酸在结肠中,炎症反馈系统与肠道微生物因子的作用有些不同。而肠道菌群对T细胞的发育和功能有更大的影响,是核受体CAR对小肠。
炎症在人体中既有积极作用也有消极作用。它可以破坏组织,但它也抑制癌症生长和对抗感染。目前的抗炎治疗会在全身系统地关闭它。这可能会带来严重的潜在后果,比如降低对感染的抵抗力或减缓对癌症的抑制。他说,在可行的情况下,将炎症疾病的治疗仅指向受影响的组织将是更好的。
孙德鲁德说:“在美国,大约有5000万患有某种自身免疫性疾病或慢性炎症的人,在医学上都接受了相同的治疗。”“圣杯会想出药物治疗的方法吗炎症只在特定的组织中留下其他的免疫细胞并能抵御癌症和微生物感染。”








用户评论