寄生虫性心脏病的实验性治疗也可能有助于阻止COVID-19
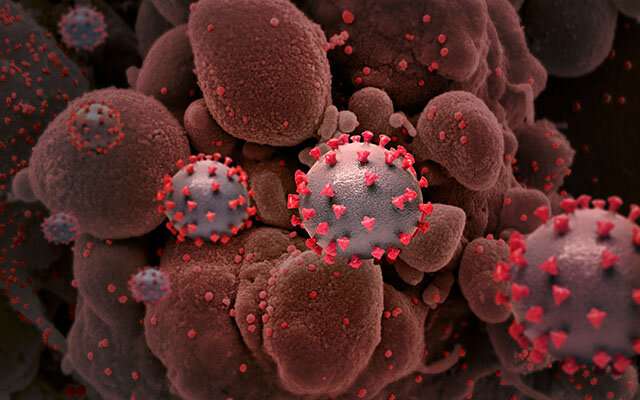
加州大学圣地亚哥分校斯卡格斯药学和药学科学学院院长、医学博士James McKerrow长期以来一直在研究被忽视的热带病——主要影响发展中国家贫困和服务不足社区的慢性和致致性寄生虫感染。它们被称为“被忽视”,因为制药公司几乎没有经济动力来开发针对它们的治疗方法。
其中一种被忽视的疾病是南美锥虫病,它是拉丁美洲心脏衰竭的主要原因,由携带寄生虫的“接吻虫”传播鲁兹锥体.这些寄生虫产生一种叫做cruzain的酶,帮助它们复制和逃避人体免疫系统.McKerrow的研究小组正在寻找cruzine的抑制剂——一种可能构成新型抗寄生虫药物基础的小分子。一种特别有效的cruzain抑制剂叫做K777。
然后,在2020年春天,COVID-19大流行开始席卷美国。研究人员很快报告说,导致COVID-19的冠状病毒SARS-CoV-2不能对接和感染人类细胞除非一种叫做组织蛋白酶L的人类酶能裂解病毒的刺突蛋白。
恰好组织蛋白酶L的外观和作用都很像cruzain。
在2021年3月31日发表的一项研究中ACS化学生物学McKerrow等研究表明,低浓度的K777抑制组织蛋白酶L可以降低SARS-CoV-2感染四种宿主的能力细胞系,而不会损害细胞.
“由于K777抑制的是一种人类酶,而不是病毒本身,我们希望病毒不太可能进化出对它的耐药性,”McKerrow说,他是该研究的共同高级作者,来自德克萨斯A&M大学的Thomas Meek博士。
K777在所有细胞系中并不是同样有效。这可能是因为并非所有细胞系都产生等量的组织蛋白酶L或等量的ACE2,病毒的刺突蛋白在被组织蛋白酶L切割后用来锁定细胞的宿主细胞受体。在产生最多组织蛋白酶L和ACE2的细胞中,抑制剂最能预防SARS-CoV-2感染。
所测试的细胞系来源于非洲绿猴肾上皮、人宫颈上皮和两种类型的人肺上皮。虽然这是一种重要的研究工具,但这样的细胞系并不一定能代表患者。它们很容易在实验室里培养和操作,因为它们是癌细胞,但这也意味着它们的分子特征可能与普通人的健康肺细胞或宫颈细胞不同。
McKerrow说:“我们对K777在实验室中阻止病毒感染的效果感到惊讶。”“然而,在通常情况下,我们自己也不太可能如此迅速地将这种化合物投入临床试验,这是不切实际的。我们很幸运,加州大学圣地亚哥分校的‘企业家驻校’项目帮助缩小了这一差距。”
一家私营生物技术公司Selva Therapeutics已经从加州大学圣地亚哥分校获得了K777的许可。在这项研究的同时,该公司还发现,这种实验性治疗方法可以防止COVID-19动物模型中的肺损伤,并且参加I期临床试验以评估安全性的人对其耐受性良好。Selva计划于2021年底在非住院COVID-19患者中进行IIa期临床试验。
许多COVID-19患者病情轻微,在支持性护理帮助缓解症状的情况下可以在家康复。目前,COVID-19严重病例可使用美国食品和药物管理局(FDA)批准用于住院患者的抗病毒药物瑞德西韦(remdesivir)治疗,或已获得FDA紧急使用授权的药物,如单克隆抗体。在全球范围内,已有超过1.24亿人被诊断患有COVID-19, 272万人死于感染。
进一步探索














用户评论