基因疗法在儿童失明患者的初步试验中显示出了希望
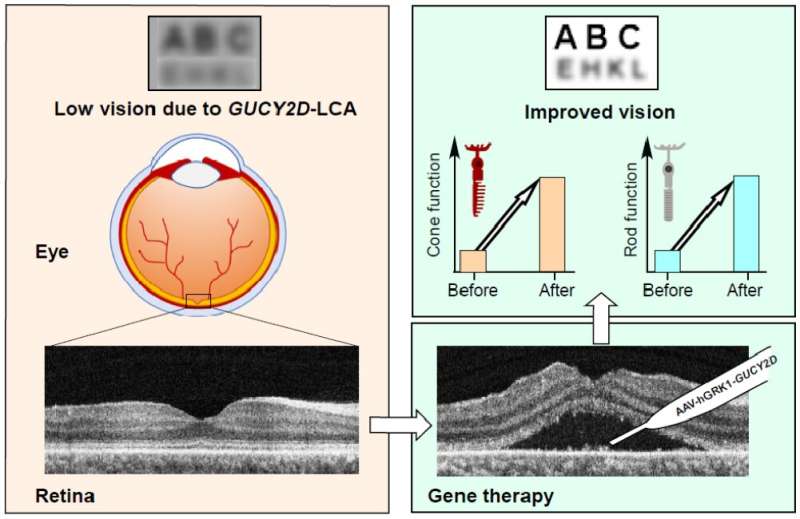
宾夕法尼亚大学(University of Pennsylvania)佩雷尔曼医学院(Perelman School of Medicine) Scheie眼科研究所(Scheie Eye Institute)的研究人员领导的一项临床试验的初步数据显示,一种针对最常见的先天性失明之一的新基因疗法是安全的,并改善了患者的视力。
的治疗将GUCY2D的工作拷贝发送到重度患者的眼睛愿景由基因突变引起的损伤。前三名接受治疗的患者在视力的某些方面都有改善,但没有严重的副作用根据新的研究报告,在期刊上发表iScience。
“我们发现,即使使用相对较低的剂量,白眼和夜视能力都有持续的改善。基因治疗该研究的主要作者塞缪尔·g·雅各布森(Samuel G. Jacobson)说,他是医学博士,佩雷尔曼医学院的眼科教授。
GUCY2D基因是25种不同人类基因中的一种基因谁的突变导致视网膜问题,导致出生或幼儿早期的严重视力障碍。这种遗传性视网膜障碍的家庭,统称为Leber先天性生物症(LCA),占全世界儿童的相当面临的失明。
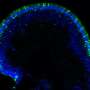
Gucy2D的正常拷贝在光敏杆和锥体的关键途径中编码酶细胞用来将光转换成电化学信号。缺乏这种酶会阻碍这一途径的恢复,阻止进一步信号传导所需的重置。结果,来自视杆细胞和视锥细胞的信号变得非常弱,相当于严重的视力丧失。
即使在患有这种疾病几十年的成年人中,通常情况下,许多感光视网膜细胞在功能障碍的情况下仍然存活和完整。因此,通过基因治疗添加GUCY2D的功能副本可以让这些细胞重新工作,并恢复一些视力。
2019年,阿图尔诉Cideciyan雅各布森和联合研究员,博士,研究在佩雷尔曼医学院眼科教授,开始第一个GUCY2D基因治疗的临床试验,一个解决方案的一种无害的病毒携带基因和注入retina-initially下每个病人在一只眼睛。他们在治疗后跟踪每个病人两年。在这份新的报告中,他们描述了对前三名患者九个月治疗后的发现。
第一个病人的杆状细胞的光敏性显著增加,杆状细胞比锥状细胞更敏感,主要负责低光或“夜视”。该病人的瞳孔对光的反应也有所改善。
第二名患者在基因治疗后两个月,杆状细胞的光敏性出现了较小但持续的增加。
第三个病人的杆细胞敏感性没有改善,但是有明显的改善视敏度在9个月的随访期内,研究人员认为患者的功能得到了改善锥形细胞,主要的日光和色彩视觉细胞。
Cideciyan说:“第一次GUCY2D基因治疗试验的初步结果非常令人鼓舞,并将为我们正在进行的和未来的这种治疗试验提供信息。”
没有严重的不良反应,患者视网膜的任何副作用都消退了。
前三名患者使用的基因治疗剂量是研究人员计划在研究中使用的最低剂量,因此他们希望在以后加入的接受更高剂量的患者中看到持续的安全性和更大的疗效。
正在进行的临床试验在clinicaltrials.gov上注册为试验NCT03920007。
雅各布森和Cideciyan在早期的研究中报道了基因治疗其他两种涉及其他基因的莱伯氏先天性黑蒙的成功。
进一步探索













用户评论