神经元-肌肉相互作用的小型化模型为ALS提供了新的视角
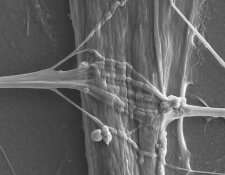
骨骼肌能够自主运动,并由一种称为运动神经元的特殊神经元控制,运动神经元通过所谓的神经肌肉连接(NMJs)与骨骼肌直接接触。正是通过NMJs,骨骼肌接收到使其收缩或放松的信号。在某些神经退行性疾病中,如肌萎缩性侧索硬化症(ALS), NMJs被破坏,导致进行性肌肉无力,最终死亡。ALS的治疗主要集中在缓解症状,但不能阻止或逆转其疾病进展。
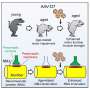
为了找到更有效的治疗方法,研究人员需要准确且易于获取的ALS实验室模型,以了解其病因,并开发和测试新的治疗方法。比利时的Ludo Van Den Bosch及其同事在这个方向上迈出了一步,他们在一种所谓的微流体装置中产生了人体外的NMJs。在这个复杂的模型中,人类运动神经元这些基因来源于ALS患者,通过诱导多能干细胞由他们自己的皮肤细胞和人类细胞改造而成骨骼肌来自健康供体的细胞生长在装置两侧的独立小室中,通过微小的通道连接两个小室。
令人兴奋的是,随着时间的推移,神经元开始发送连接,称为轴突,通过通道形成NMJs,这些NMJs能够将信号从神经元传递到肌肉细胞,类似于大脑中的NMJs人体.然而,当将ALS患者的运动神经元与健康的运动神经元进行比较时,很明显,ALS运动神经元通过通道发送的轴突更少,与肌肉细胞形成的NMJs也更少。此外,ALS运动神经元对受损轴突的再生效率较低。令人鼓舞的是,通过在培养物中加入化学物质Tubastatin A, ALS运动神经元可以生长出更多的轴突,达到与健康运动神经元相似的水平。进一步的研究将显示Tubastatin A是如何抑制细胞中某一类蛋白质,促进ALS运动神经元轴突生长的,以及是否可以在动物模型和最终在ALS患者中实现类似的效果。
这个新的NMJ形成的小型化模型最近发表在干细胞报告,将在研究运动神经元病理和发现ALS的潜在治疗方法方面得到广泛应用。
进一步探索












用户评论