被发现可以控制正常生长和癌症的驱动因子
研究人员发现了一种长期寻找的酶,它可以通过分解驱动细胞生长的蛋白质来预防癌症,而当细胞失去功能时,这种酶就会导致癌症。
发布在网上自然4月14日,新的研究围绕着每个人类细胞一分为二的能力展开单个细胞(受精卵)变成一个有数万亿个细胞的身体。细胞每次分裂都必须遵循一定的步骤,其中大部分都是由一种叫做细胞周期蛋白的蛋白质促进的。
由纽约大学格罗斯曼医学院(Grossman School of Medicine)的研究人员领导的这项研究揭示了一种名为AMBRA1的酶标记了一种关键的细胞周期蛋白,这种细胞周期蛋白可以被分解蛋白质的细胞机器所破坏。这项研究发现,这种酶对细胞周期蛋白的控制对于胚胎发育过程中细胞的正常生长至关重要,而这种酶的功能失常会导致致命的细胞过度生长。此外,该研究进一步表明,现有的药物类别可能能够在未来扭转这种缺陷。
与发育中的胎儿一样,抑制细胞分裂是预防癌症中出现的异常、侵略性生长的关键。新的研究发现,细胞已经进化到使用AMBRA1来防御这种生长。
“我们的研究阐明了人类细胞的基本特征,提供了见解癌症生物学并开启新的研究途径进入潜在的治疗方法,“Nyu Langone Health的生物化学和分子药理学系的主席,MICHELE Pagano,MICH,以及与Howard Hughes Medical Institute的调查员。
新的肿瘤抑制
目前的研究针对的是三种d型细胞周期蛋白,如果细胞要分裂,它们必须与称为细胞周期依赖激酶(CDKs)的酶连接,特别是CDK4和CDK6。作者发现,AMBRA1作为一种连接酶,将分子标记附在所有三种d型细胞周期蛋白上,标记它们是否被破坏。以前提出的d型细胞周期蛋白如何被细胞消除的机制无法被科学界复制。Pagano说,因此,在这项新研究之前,d型细胞周期素的一个中央调控因子已经存在了四分之一个世纪。
这项新研究还揭示了AMBRA1在生物发展中的作用。缺乏AMBRA1基因(AMBRA1酶的编码基因)的老鼠,产生了不受控制的、致命的组织生长,扭曲了发育中的大脑和脊髓。研究人员还首次发现,用CDK4/6抑制剂治疗携带没有AMBRA1基因胚胎的怀孕小鼠,减少了这些神经元异常。
而言,癌症,作者分析了患者数据库以得出结论,ambra1低于正常表达的人不太可能存活弥漫性大B细胞淋巴瘤,这是美国的非霍奇金淋巴瘤的最常见形式。Ambra1的较低表达的原因可以包括删除基因的随机变化或使其编码指令更难读取。
为了证实AMBRA1作为肿瘤抑制因子的作用,研究人员与宾夕法尼亚大学的研究作者Luca business博士合作,监测了弥漫性大b细胞淋巴瘤小鼠模型中的癌细胞生长。当人类b细胞淋巴瘤细胞例如,不携带AMBRA1基因的肿瘤比携带该基因的肿瘤生长速度快三倍。纽约大学朗格尼领导的研究着眼于弥漫性大b细胞淋巴瘤,斯坦福大学和丹麦癌症协会研究中心领导的另外两项研究发表在同一杂志上自然研究发现,AMBRA1缺失或缺失是导致肺癌的关键因素。
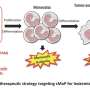
此外,已知d型细胞周期蛋白与CDK4和CDK6组装成鼓励正常和异常的酶细胞生长。近年来,抑制CDK4和CDK6的药物已被fda批准作为癌症治疗药物,但一些患者对这些药物的反应较弱。为了深入了解这个问题,目前的研究小组发现,缺乏AMBRA1的淋巴瘤对CDK4/6抑制剂的敏感性较低。当AMBRA1基因缺失时,d型细胞周期蛋白的水平变得足够高,可以与另一种CDK (CDK2)形成复合物,由于其结构,CDK4/6抑制剂不能使其失活。
“这使得AMBRA1成为选择最适合CDK4/6抑制剂治疗的患者的潜在标记物,”第一作者Daniele Simoneschi博士说,他是纽约大学朗格尼健康中心生物化学和分子药理学高级研究协调员。下一步,他说,研究小组计划研究CDK4/6抑制剂和CDK2抑制剂在低AMBRA1肿瘤中的作用,以及那些d型细胞周期蛋白突变使其对AMBRA1不敏感的肿瘤。
进一步探索













用户评论