靶向异常细胞代谢显示治疗小儿脑肿瘤的承诺
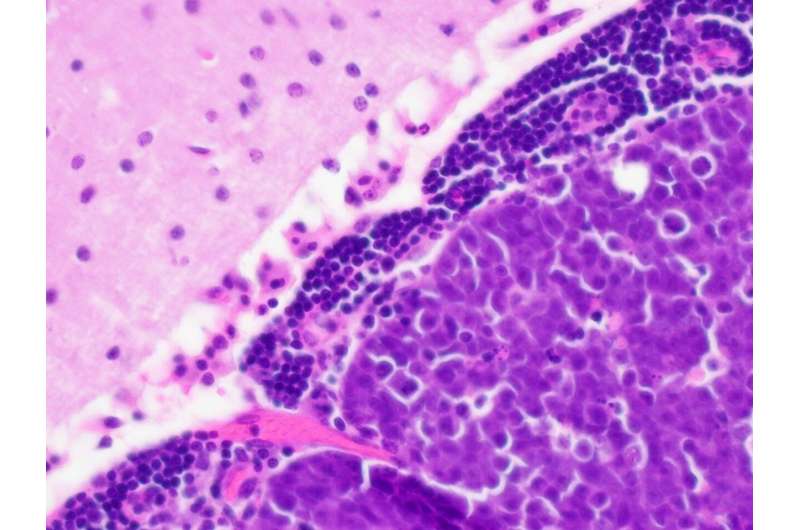
两种实验药物方法,癌细胞代谢的毒性脆弱性可能会延长存活率并提高标准化学疗法的有效性,以获得高度侵略性的小儿脑癌。
约翰霍普金斯金梅尔癌症中心研究人员在两个公布的研究中报道了调查结果。
髓母细胞瘤是儿童最常见的恶性脑肿瘤瘤。肿瘤患者的一部分称为第3组MYC-SAMALIED成神经管细胞瘤总生存率小于25%。在这些患者中,通过改变癌细胞代谢来改变癌症细胞生长的癌症促进Myc癌症。癌症细胞利用能量的方式不同于正常细胞,因此它们可能容易受到靶向MYC下游异常代谢途径的治疗。
在第一次研究中,3月22日发布神经病理学与实验神经病学Eric Raabe, M.D, Ph.D.,约翰霍普金斯大学医学院肿瘤学副教授,专注于代谢改变药物DON (6-diazo-5-oxo-L-norleucine)。DON是一种用于成人和儿童癌症研究的天然化合物临床试验自20世纪80年代以来,它从未对Myc驱动的脑肿瘤进行了系统地测试过。
虽然Don在早期癌症临床试验中的儿童安全,但目前临床上没有。
由Barbara Slusher,博士,硕士,约翰霍普金斯药物发现主任和约翰霍普金斯大学医学院神经学教授领导的研究小组,修改了DON以增加它穿过血脑屏障的能力,创造了一种DON前药,JHU395。在前药中,化学成分发生变化,因此药物仅在癌细胞。
“唐前药的承诺是制定一个不会受伤的治疗方法正常细胞但可以在脑癌细胞中优先释放,“拉贝说。
在一组实验中,研究人员用JHU395和DON处理人类高myc髓母细胞瘤细胞株。他们发现,与单独使用DON相比,前药在较低浓度下能有效抑制癌细胞生长并杀死癌细胞。
接下来,用JHU395治疗携带植入人髓母细胞瘤肿瘤的小鼠。研究人员发现该治疗导致了对Myc驱动的癌细胞的选择性杀死,而正常的脑细胞被施加。此外,JHU395治疗显着延长了生存率。在给定安慰剂的小鼠中,处理的小鼠几乎没有两倍。
“Jhu395同样有效,因为唐少剂量,因为它具有更好的脑癌细胞渗透,”Raabe说。“随着潜在减少的副作用来提出新的治疗意味着我们可以将毒品结合起来更好的患者生存,这就是这一切的全部。”
在第二项研究中,2月8日在线发布癌症字母, Raabe和他在其他三个癌症研究机构的同事们以参与细胞代谢的哺乳动物雷帕霉素复合物为目标。mTOR蛋白向癌细胞发出生长信号,侵入健康组织并抵抗治疗。
先前的研究表明,除了MYC高表达外,侵袭性儿童成神经管细胞瘤也有高水平的mTOR表达,这使得研究者认为mTOR抑制剂可能具有治疗价值。Raabe说,一种生物信息学药物筛选确定了TAK228(也被称为sapanisertib),一种穿透大脑的mTORC1/2激酶抑制剂,可能是一种对儿童有效的制剂。
研究人员发现,Tak228抑制MTORC1 / 2,抑制肿瘤细胞生长高达75%,有效地杀死了MYC驱动的人髓母细胞瘤癌细胞。
接下来,调查人员侧重于测量MYC驱动的髓质细胞瘤的异常代谢。在癌症中,升高的谷胱甘肽是一种手段,肿瘤细胞对化疗抵抗力。谷胱甘肽专门允许细胞阻断含有铂的化疗药物的效果,例如顺铂和卡铂。这些含铂的药物是Medulloblastoma治疗的一些主要成分。在小鼠中生长的人髓母细胞瘤中,Raabe和同事发现肿瘤细胞具有比正常脑细胞更多的谷胱甘肽。使用多余的谷胱甘肽可能是这些癌细胞抵抗化疗的一种方式。
研究人员发现,TAK228 MTOR抑制剂中断并降低了癌细胞中的谷胱甘肽合成。当它们对患有高myc medulloblastoma脑肿瘤的小鼠与Tak228和卡铂的组合进行了治疗,组合有效地杀死了肿瘤细胞,而不是单独使用的药物延长存活。用组合疗法治疗的小鼠几乎只需对照小鼠的两倍。在组合治疗的小鼠中,20%被认为是非常长的幸存者,在实验开始后近80天生活,而所有对照小鼠在25天内从其肿瘤中死亡。
“通过瞄准MTOR途径,TAK228克服了一个关键电阻机制癌症细胞必须传统化疗,“Raabe说。”这些Myc驱动的癌症制作了很多谷胱甘肽 - 它们的生长如此之快他们需要很多。Tak228减少了他们可以制造的量,使它们易于化疗。“
他补充说:“这是未来mTOR抑制剂联合传统化疗儿童临床试验中有价值的临床前数据,它可能最终改变儿童被诊断为myc驱动的髓母细胞瘤的结果。”
进一步探索
Rachael E. Maynard等,Torc1 / 2激酶抑制耗尽谷胱甘肽并用卡铂促进Myc驱动的Medulloblastoma的生长,癌症字母(2021)。DOI:10.1016 / J.Canlet.2021.02.001










用户评论