研究人员更接近基因疗法,以恢复先天失聪的听力
俄勒冈州立大学的研究人员在寻求使用基因治疗方面发现了一个关键的谜题,使人们出生的聋人听到。
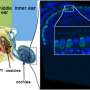
这项工作的中心是一个负责内耳蛋白质——耳铁蛋白的大基因。耳铁蛋白的突变与严重的先天性听力损失有关,这是一种常见的耳聋类型,患者几乎听不到任何东西。
俄勒冈州立大学理学院生物化学和生物物理学副教授科林·约翰逊说:“很长一段时间以来,耳铁蛋白似乎是一种只有一招的蛋白质。”“很多基因威尔发现有很多事情要做,但是耳铁蛋白基因似乎只有一个目的那就是在感觉毛孔在内耳。耳铁蛋白的微小突变会使人严重失聪。”
在其常规形式中,Otoferlin基因太大而无法包装成送货车分子治疗,所以约翰逊的团队正在查看使用截断的版本。
由研究生Aayushi Manchanda领导的研究表明,缩短的版本需要包含被称为跨膜域而其中一个出乎意料的原因是:没有跨膜结构域,感觉细胞成熟缓慢。
约翰逊说:“这是令人惊讶的,因为众所周知耳铁蛋白有助于编码听觉信息,但从未被认为与感觉细胞的发育有关。”
研究结果今天发表在细胞的分子生物学。
约翰逊实验室的科学家们一直在多年与Otoferlin分子一起工作,并于2017年鉴定了一种可以在声音编码中起作用的基因的截短形式。
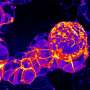
为了测试耳铁蛋白的跨膜结构域是否需要成为基因缩短版本的一部分,Manchanda引入了一个突变,截断了斑马鱼的跨膜结构域。
斑马鱼,一个小淡水种类,在大约五天内从细胞到游泳鱼,对分子,遗传和细胞水平的人类分享着一种显着的相似性,意思是许多斑马鱼发现与人类立即相关。胚胎斑马鱼是透明的,可以很容易地保持少量水。
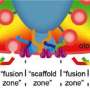
“跨膜结构域将Otoferlin与细胞膜和细胞内囊泡进行,但如果这是必要的,并且必须包含在缩短的Otoferlin形式中,”Manchanda说。“我们发现跨膜域的损失导致感官发毛细胞产生较少的耳铁蛋白和毛细胞活性的缺陷。突变也导致了成熟的延迟感觉细胞,这是一个惊喜。总的来说,结果争辩说,跨膜域必须包含在任何内容中基因治疗构造。”
在分子水平,Manchanda发现,缺乏跨膜结构域导致Otoferlin未能正确地将填充有神经递质填充到细胞膜的突触囊泡,从而释放不太神经递质。
“我们的研究表明otoferlin将囊泡固定在细胞膜是编码声音过程中神经递质释放的关键机制步骤,”Manchanda说。
进一步探索











用户评论