在出生后发育过程中维持海马神经干细胞的自我更新和增殖
发表在细胞的报道中国科学院脑科学与智能技术卓越中心、中国科学院神经科学研究所周家伟实验室、南京医科大学胡刚课题组研究表明,FGF13基因在出生后海马神经干细胞(NSCs)的自我更新和增殖过程中起着内在调节作用。
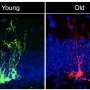
的发展海马齿状回(DG)的可塑性对学习和记忆等行为至关重要。在小鼠大脑中,DG中的颗粒细胞大部分是在出生后早期产生的。DG中NSCs的神经源性能力在出生后两周内急剧下降,成年后随着年龄的增长逐渐下降。
FGF13属于非分泌性成纤维细胞生长因子(FGFs)家族的一个亚群。人类遗传学研究显示,Fgf13是一些x -连锁脑疾病的候选基因,包括精神发育迟滞和癫痫发热性癫痫发作说明FGF13在大脑发育中起着重要作用。CEBSIT之前的一项研究表明,FGF13参与了胚胎期前脑未成熟神经元的极性/迁移调节。
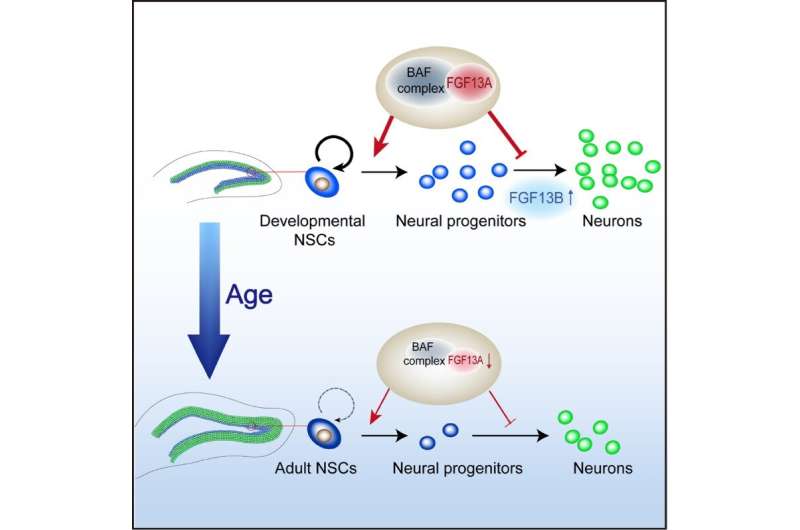
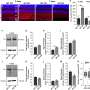
本研究发现NSCs中FGF13亚型A的表达随着DG神经发生的年龄相关性下降而降低,NSCs中FGF13的缺失导致小鼠出生后DG神经发生及海马相关学习记忆行为明显受损。
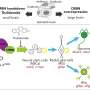
在机制上,FGF13A亚型通过修饰维持NSCs的自我更新能力是必不可少的染色质结构调节神经元分化相关的基因。酵母双杂交实验表明,FGF13A与ARID1B相互作用,从而调控NSCs的发育。ARID1B是Brahma-associated factor (BAF)染色质重塑复合体的关键成分。
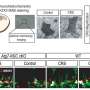
此外,转座酶可及染色质高通量测序(ATAC-seq)结果表明,FGF13是维持神经元分化相关基因染色质闭合状态,以维持神经干细胞的自我更新和增殖状态所必需的。因此,正常的海马发育需要FGF13亚型表达的时空协调。
本研究表明FGF13对于预测和干预与出生后发育和衰老相关的精神障碍具有重要意义。
进一步探索









用户评论