促进罕见遗传性听力损失患者的言语理解
听力损失是一种影响世界大约5%的人口的残疾。临床上确定病变的确切部位对于选择对听力损失的适当治疗至关重要。例如,具有声音传导或轻度外毛细胞损伤的受试者将受益于助听器,而对外部或内毛细胞具有显着损害的人将受益于耳蜗植入物。另一方面,诸如耳蜗神经,脑干或大脑等更多中央结构中具有损伤的受试者不会受益于助听器或耳蜗植入物。然而,在听力损失中的耳蜗神经胶质细胞中的损伤在听力损失中的作用也不是众所周知。虽然已知耳蜗胶质细胞的Connexin通道在培养耳蜗中的钾电流中起重要作用,但Connexin通道的分子和细胞机制及其在逐步听力损失中的作用尚未得到广泛研究。
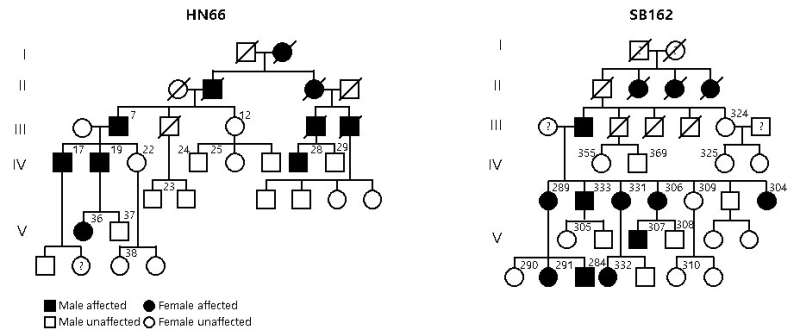
听觉神经病变谱系障碍(ANSD)是一种混淆的听觉疾病,受试者可以响应声音但在言语歧视中具有困难。最近,来自认知和社会性(IBS),首尔国立大学Bundang医院,中南大学,中南大学和迈阿密大学的研究人员的合作鉴定了导致这种疾病的先前未知的耳聋基因。新的基因TMEM43位于染色体3中,主要用胶质增长的支撑细胞(GLSs)的耳蜗。他们发现,TMEM43的p.(Arg372Ter)变异在韩国和中国两个著名的亚洲家族中遗传,这两个家族都患有ANSD。
为了研究这种疾病,研究人员使用了一种转基因小鼠模型有缺陷的TMEM43-p (Arg372Ter)基因。研究人员发现,这种老鼠模型也表现出同样的进步听力损失作为人类ANSD科目。进一步检查这些小鼠显示,与对照小鼠相比,较老小鼠的GLS细胞尺寸较小。此外,显示TMEM43蛋白与Connexin通道(CX26和CX30)相互作用,已知该蛋白质可以调节耳蜗中的K +电导。突变小鼠显着损害K +电导。基于鼠标模型的机械洞察力,研究人员对3名人ANSD患者进行了耳蜗植入物,这导致了他们的演讲歧视的成功恢复。
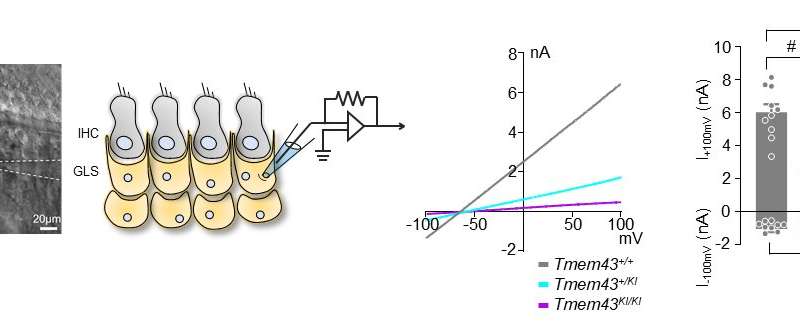
本研究值得注意的是,它们鉴定了人类的新型耳聋基因,研究了使用a的人受试者发现的遗传变异的潜在机制鼠标模型并将结果恢复到人类成功临床结果的人。因此,本研究提供了一个模型平台,其中可以确定听觉康复的个性化模型,突出了基于精密药的方法的重要性。
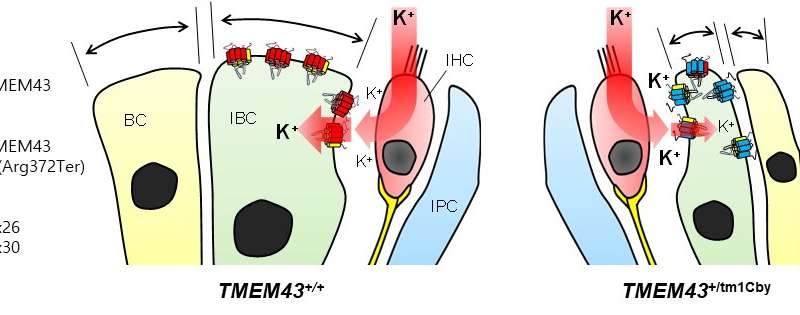
Choi Byung Yoon博士表示,“我们很兴奋地将TMEM43添加到导致耳聋的基因列表中。它将极大地有助于通过简单的遗传测试来准确诊断和定制治疗耳聋。”此外,导演C. Justin Lee提到了“这项研究强调了胶质细胞在耳蜗中的重要作用。我们积极的是进一步的研究将为许多患有这种罕见的耳聋的患者提供希望。”
作为未来的后续研究,研究人员希望招募更多具有其他ANSD基因变异的受试者,以便为这种罕见的耳聋疾病提供进一步的临床见解。基于TMEM43蛋白对耳蜗胶质细胞K+电导的贡献,研究者计划继续研究TMEM43蛋白和离子通道在大脑中的作用。
进一步探索
















用户评论