反义基因治疗的新组件表明承诺在治疗脊髓性肌萎缩

Skoltech研究者和他们的同事从俄罗斯和英国进行的安全性和有效性的新化学反义寡核苷酸治疗脊髓性肌萎缩(SMA),一种遗传性疾病。他们的研究结果可能会导致药物毒性少、注射的发展需要感谢长时间的行动。论文发表在杂志上核酸疗法。
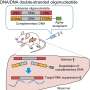
反义寡核苷酸片段的DNA单链化学修改目标pre-messenger RNA,短的基因信息比特核糖体读取蛋白质。根据一个特定的反义寡核苷酸是如何工作的,目标信使rna可以被摧毁或进行拼接的细微变化,即外显子,编码区域,排除或包含在最终的信使rna。
反义寡核苷酸擅长针对所谓的单基因疾病,在疾病的起因源于一个特定基因/蛋白质。一个常见的例子是这样的疾病脊髓性肌肉萎缩症(SMA);患有这种疾病的SMN1基因失去功能的蛋白质编码,虽然人类基因组包含一个几乎相同的副本,SMN2,这个基因的mrna转录缺乏必要只有一个外显子,导致很差的功能蛋白质。
帮助细胞成功地使用SMN2 SMN1,而是一个反义寡核苷酸可以干扰拼接成熟的前体mRNA,包括特定的外显子。这就是nusinersen,临床批准反义寡核苷酸对SMA Spinraza销售,工作。
副教授Timofei Zatsepin Skoltech生命科学中心,CLS高级研究科学家奥尔加Sergeeva及其同事研究了寡核苷酸替代phosphorothioate组织接头切换。以前,从新西伯利亚Stetsenko州立大学博士开发了与甲磺酰寡核苷酸(mesylµ)或1-butanesulfonyl (busylβ)phosphoramidate组。
“Phosphorothioate是关键化学改性开发的核酸Fritz Eckstein教授在1960年代后期,存在于几乎所有的寡核苷酸药物批准为止。它可以提高稳定性、药效学和药物动力学的寡核苷酸,但展示了明显的毒性,限制了应用寡核苷酸药物。在过去的30年里,许多替代品开发,但我们确实相信mesyl phosphoramidates优于其他治疗寡核苷酸磷酸模仿,”Zatsepin说。
这些新的化合物有点不同寻常的,因为它们的结构很困惑当一看到第一次的公式。“你认为这样批量组应该强烈干扰细胞内所有交互。博士领导的,然而,我们的同事来自新西伯利亚德米特里•Stetsenko之前证明µ-oligonucleotides比PS寡核苷酸更少有毒,而工器与DNAµ-oligonucleotides良好的核糖核酸酶底物的信使rna降解的关键酶通过反义机制,”Zatsepin指出。
研究人员受这些结果,看起来,除此之外,对接头切换寡核苷酸与潜在的长期行动。Nusinersen管理几次每年通过注射进入椎管,所以少注射会提高SMA患者的生活质量。
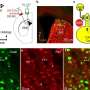
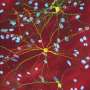
团队能够测试活动的小说反义寡核苷酸在SMA patient-derived成纤维细胞在体外和体内的新生儿SMA的小鼠模型。“在我们的研究中我们发现,µ-oligonucleotides活性体外,体内功效较低时相比nusinersen在同一剂量。µ-oligos更稳定和更少的有毒比PS寡核苷酸在体内,我们建议µ-oligos中使用高剂量可以提供相同的功效与更多长期动作这研究是正在开发的现在,”Zatsepin解释道。
更多信息:苏珊·m·哈蒙德et al, Mesyl Phosphoramidate寡核苷酸作为潜在Splice-Switching代理人:主体结构对活性和细胞内定位的影响,核酸疗法(2021)。DOI: 10.1089 / nat.2020.0860