维生素A衍生物可提高放疗的肿瘤杀伤效果

放射治疗是癌症治疗的一个重要组成部分,50%到60%的癌症患者使用放射治疗。传统上,它被用于局部癌症,如头颈癌、宫颈癌、前列腺癌、肺癌和脑癌,都有不同程度的成功。
芝加哥大学医学综合癌症中心的研究人员领导的团队发现,放疗与全反式维甲酸(ATRA)的结合不仅能显著抑制局部放疗肿瘤的生长,也能显著抑制未接受放疗的远端肿瘤的生长。放疗和ATRA联合治疗可调节肿瘤微环境增强了辐射对局部和全身的影响。
“我们的团队是第一个将ATRA和放疗结合起来治疗的团队实体肿瘤Ralph Weichselbaum医学博士、Daniel K. Ludwig杰出服务教授、放射和细胞肿瘤学主席和该研究的资深作者说,该研究发表在2021年6月11日的《美国癌症杂志》上科学免疫学。
ATRA是维生素a的一种形式,被认为在免疫相关细胞的发育和分化中发挥作用。它已被FDA批准用于治疗急性早幼粒细胞白血病(一种侵袭性血癌),被认为是一种比化疗更有效、毒性更小的治疗方法。
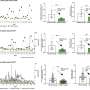
Weichselbaum和一个由基础科学和临床研究人员组成的多学科小组发现,ATRA和放疗联合使用产生的抗肿瘤反应比放疗或单独使用ATRA产生的抗肿瘤反应大得多。
仅靠辐射,一些肿瘤的炎症就会促使单核细胞(一种白细胞)赶到现场修复损伤。然而,在肿瘤微环境中,这些单核细胞中的一些被重新编程为骨髓来源的抑制细胞(MDSCs),它促进肿瘤生长,抑制T细胞的肿瘤杀伤能力。
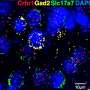
“ATRA的加入反而创造了一个正反馈循环,”芝加哥大学的研究助理教授、论文的共同资深作者Hua Laura Liang博士解释道。当受到照射时,肿瘤原有的T细胞开始产生干扰素γ (IFN-γ),这对激活免疫反应很重要。IFN-γ和ATRA一起将有害MDSCs的浸润单核细胞转化为有益的炎症巨噬细胞,产生高水平的两种强大的信号蛋白:诱导NO合成酶(iNOS)和肿瘤坏死因子α (TNF-α)。这些巨噬细胞和它们产生的蛋白质进一步刺激肿瘤微环境,从而吸引更多的T细胞,开始新的循环。
“我们可以取促进细胞肿瘤的生长并将它们重组为增强抗肿瘤免疫的细胞,”Weichselbaum说。
值得注意的是,联合治疗不仅激活了杀死癌细胞的CD8+ T细胞,还激活了CD4+ T细胞,CD4+ T细胞是在抗肿瘤免疫中起关键作用的“助手”细胞。两种类型的T细胞产生的IFN-γ水平升高,IFN-γ介导癌细胞杀伤。
值得注意的是,CD8+和CD4+ T细胞的数量不仅在局部照射过的肿瘤中增加,在远端未治疗的肿瘤中也增加,这种现象被称为异位效应。
此外,研究小组能够通过在联合治疗中添加PD-L1阻断剂进一步抑制远端肿瘤的生长,PD-L1阻断剂是一种免疫治疗药物,可以让T细胞识别和杀死肿瘤肿瘤细胞.Weichselbaum说:“PD-L1阻断剂的加入产生了更强的异位效应。”
该团队认为,他们的发现不仅可以用于atra影响的免疫细胞分化的进一步研究,还可以用于临床试验中的长凳到床边的翻译。“这项工作具有潜在的临床意义,使用ATRA作为t细胞靶向化合物,改善放疗的局部和全身效果,从而使转移患者受益癌症”,Weichselbaum总结道。
进一步探索