发现靶向药物对抑制胰腺肿瘤有效

胰腺癌是一种侵袭性疾病,恶性细胞在胰腺组织中形成。胰腺是位于胃后方的一个长而平的腺体,有助于消化和血糖调节。根据美国国家癌症研究所(National cancer Institute)的数据,由于胰腺癌很难在早期被发现,它的生存率很低,仅占美国所有新发癌症病例的3%多一点,但导致的死亡人数却占所有癌症死亡人数的近8%。
通过预临床研究他曾在莫菲特癌症中心工作,并于临床癌症研究赛德·塞布提博士是弗吉尼亚州立大学梅西癌症中心基础研究副主任,他发现了一种新型药物,可以有效地抑制癌症胰腺肿瘤是上瘾的癌症导致突变KRAS基因。Sebti最近与Massey的临床同事会面,讨论如何评估该药物临床试验在病人身上胰腺肿瘤藏匿突变KRAS。
Sebti说:“我们发现了CDK蛋白的过度激活和突变KRAS成瘾之间的联系,我们在临床前利用这一联系来对抗突变KRAS驱动的胰腺癌,为患有这种致命疾病的患者进行临床研究提供了证据。”Sebti也是梅西大学癌症研究的莱西家族主席,也是VCU医学院的药理学和毒理学教授。“我们的发现非常重要,因为它们揭示了一种新的途径来对抗一种侵袭性胰腺癌,这种胰腺癌的预后非常差,主要是由于它对传统疗法的耐药性。”
KRAS在90%的胰腺癌中都有突变。Sebti实验室和其他实验室先前的研究已经证明,一些含有突变KRAS的肿瘤实际上对突变基因上瘾,这意味着没有突变基因它们就无法生存或生长。Sebti开始研究是否有一种药物可以特异性地杀死对突变KRAS上瘾的肿瘤。
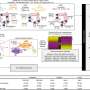
Sebti和合作者用三种科学方法试图回答这个问题。
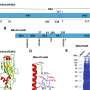
首先,他们通过全球磷蛋白组学绘制了胰腺癌细胞的蓝图,这让他们了解了上瘾和非上瘾肿瘤在磷蛋白水平上的差异。他们发现了两种蛋白质——cdk1和cdk2——这表明哪些细胞对突变KRAS上瘾。
此外,他们还分析了麻省理工学院布罗德研究所和哈佛大学的一个综合数据库,其中包含全基因组CRISPR gRNA筛选数据集。他们发现CDK1和CDK2以及CDK7和CDK9蛋白与突变的kras成瘾肿瘤相关。
最后,他们评估了294种FDA药物库在实验室中选择性杀死突变kras成瘾癌细胞而非kras成瘾癌细胞的能力,并确定临床前实验中最有效的药物是AT7519,一种CDK1, CDK2, CDK7和CDK9的抑制剂。
Sebti说:“使用三种完全不同的方法,我们清楚地得出了相同的结论:肿瘤对突变KRAS上瘾的胰腺癌患者可以从CDK抑制剂AT7519的治疗中获益很大。”
为了在来自胰腺癌患者的新鲜肿瘤中进一步验证这些发现,Sebti与首席外科医生Jose Trevino医学博士和当时在佛罗里达大学的Massey肿瘤学杰出教授Walter Lawrence Jr.合作进行了这项研究。他们发现AT7519抑制了五个突变KRAS胰腺癌患者的异种移植细胞的生长,这些患者在化疗和/或放疗治疗中复发。
AT7519此前在一些临床试验中测试不成功,但没有一项试验针对胰腺癌。
Sebti说:“如果我们的发现是正确的,并转化为人类,那么我们应该能够在肿瘤对突变KRAS上瘾的胰腺癌患者身上看到积极的反应。”
该研究的作者认为,除了胰腺癌这些发现也可能对KRAS突变普遍存在的结直肠癌和非小细胞肺癌患者具有临床意义。
进一步探索