自噬报告鼠提示未来治疗,康复策略
肌肉组织的丧失——医学上称为肌肉萎缩——可能是由于长时间缺乏体力活动的结果;老化;酒精相关肌病——由于长时间过度饮酒导致的肌肉疼痛和无力;烧伤;伤害;营养不良;脊髓或周围神经损伤;中风;以及长期的皮质类固醇治疗。虽然由于废用引起的肌肉萎缩是众所周知的和研究的,但其潜在的细胞机制,特别是废用引起的肌肉萎缩中线粒体线粒体降解的状态,一直是细胞生理学家争论的主题,因为线粒体在骨骼肌中丰富。
线粒体分裂是一种细胞质量控制机制,通过它细胞分解被称为线粒体的受损或功能失调的亚细胞细胞器。虽然线粒体在细胞能量生产和其他细胞内稳态功能中起着至关重要的作用,但在废用诱导的肌肉萎缩过程中,线粒体释放活性氧(ROS)已经有过报道。据认为,ROS氧化蛋白质、脂质和核酸导致蛋白质分泌减少,最终导致肌肉萎缩。
来自新泻大学医学与牙科科学研究生院细胞生理学系的一组研究人员与大正制药株式会社和日本国家量子与放射科学技术研究所合作,开发了一种新的荧光报告鼠系,用于检测细胞的变化mitophagy可以改善治疗策略的活动,并可能促进逆转因废用引起的肌肉萎缩的策略。
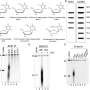
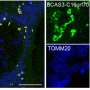
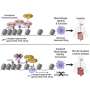
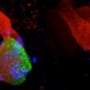
在一项小鼠模型研究中,作者设计了利用双mCherry/EGFP(红/绿)报告器的体内荧光方法,以可视化后肢固定(后肢IM)小鼠肌肉组织切片的线粒体变化(如图,右)。他们跟踪了共表达绿色EGFP和红色mCherry蛋白的胞质线粒体的存在,然而,当线粒体在有丝分裂条件下被运送到溶酶体形成有丝分裂溶酶体时,绿色EGFP蛋白被淬灭和降解,从而可以直接分析体内的有丝分裂活性。
虽然之前有研究使用了其他的自噬分析方法,Keiichi Inoue博士和Tomotake Kanki教授详细阐述了他们的方法的不同之处,他们说:“我们新的报告鼠系列能够直接分析体内的自噬活性。这比以往基于自噬标记基因表达的间接方法更有利,因为这些基因对自噬诱导没有特异性。”这种双荧光报告系统可以直接和特异性地监测体内自噬活性。
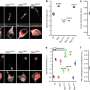
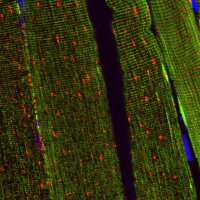
作者在研究与废用诱导的萎缩肌肉相关的自噬变化时,使用新的报告小鼠评估了自噬活性。他们报告了14天后肢固定后萎缩比目鱼肌中细胞自噬活性水平和ROS水平的增加,显示肌肉废用增加了细胞自噬活性骨骼肌.
该研究强调线粒体吞噬是废用性肌肉萎缩的潜在治疗靶点。此外,随着肌肉萎缩是伴随生理性老化还是一些病理状态,如肌病或神经病变,这种新模式是否有助于了解和预防肌肉萎缩遵循这些变化。
“我们将进一步揭示自噬在其他生理和病理后果中的动态,”作者写道。
进一步探索