纠正致病突变的新技术
基因编辑,或故意改变基因的DNA序列,是一个功能强大的工具,研究突变导致疾病,并能改变个体的DNA用于治疗目的。小说的方法可以用于两个目的基因编辑已经办事,领导的研究小组开发的詹姆斯w(1963)和帕特里夏·t·Poitras麻省理工学院脑与认知科学教授。
“这技术进步可以加速疾病模型动物的生产,关键的是,开辟了一个全新的方法纠正致病突变,”冯说,世卫组织还广泛的哈佛和麻省理工学院的一员,麦戈文脑研究所副主任在麻省理工学院。新的研究结果发表在《华尔街日报》细胞。
遗传疾病的模型
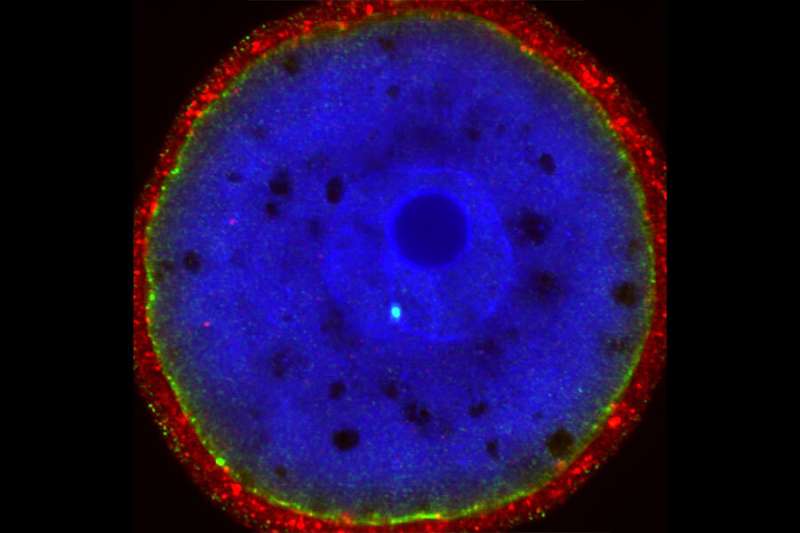
冯实验室的一个主要目标是精确定义出错在神经发育和神经精神障碍工程动物模型,把人类基因突变导致这些障碍的。新模型可以通过注射胚胎生成基因编辑工具,以及一段DNA携带所需的突变。
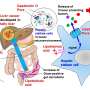
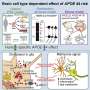
在这样一个方法中,基因编辑工具CRISPR编程削减目标基因,从而激活天然DNA机制,“修复”破碎的基因注入模板DNA。然后使用基因工程细胞产生后代的能力进一步通过遗传变化给后代,创造一个稳定的遗传疾病的治疗,进行测试。
尽管CRISPR加速生成这样的疾病模型的过程中,这个过程可能还需要几个月或几年。效率低下的原因,许多治疗细胞不进行所需的DNA序列改变,和这两个基因的变化只发生在一个副本(对于大多数基因,每个单元格包含两个版本,一个来自父亲,一个来自母亲)。
为了增加基因编辑过程的效率,冯实验室团队最初假设添加一个DNA修复蛋白RAD51 CRISPR基因编辑工具的标准混合物的可能性将会增加一个细胞(在这种情况下小鼠受精卵中,或一个细胞的胚胎)将进行所需的基因变化。
作为一个测试用例,他们测量了他们能够插入的速度(“敲入”)的突变基因Chd2与自闭症有关。总体比例的胚胎正确编辑保持不变,但令他们吃惊的是,一个更高比例进行所需的染色体基因编辑。测试一个不同的基因产生了意想不到的结果是相同的。
“编辑两个染色体的同时通常是非常罕见的,”解释了博士后乔纳森·王尔德。“编辑的高速率与RAD51非常引人注目,什么开始作为一个简单的试图使突变Chd2老鼠迅速变成了一个更大的项目集中在RAD51及其在基因组编辑、应用“王尔德说,合著的文章细胞研究科学家Tomomi阿依达。
一个分子复印机
冯实验室团队接下来着手了解的机制RAD51增强基因编辑。他们推测,RAD51参与这一过程被称为interhomolog修复(《国际卫生条例》),即一条染色体上DNA断裂修复使用第二份染色体(从其他家长)作为模板。
为了验证这一点,他们注射小鼠胚胎和RAD51 CRISPR但模板DNA。他们编程CRISPR削减只有基因序列的染色体,然后测试是否修理毛边的染色体的序列相匹配。对于这个实验,他们不得不使用老鼠的父系和母系的染色体序列是不同的。
他们发现,控制胚胎注射CRISPR很少单独显示国际卫生条例修复。然而,添加RAD51显著增加数量的胚胎CRISPR-targeted基因编辑与毛边的染色体。
”《国际卫生条例》之前的研究发现,在大多数细胞的效率非常低,“王尔德说。“我们发现它更容易发生在胚胎细胞,可以增强RAD51表明,更深入地理解胚胎的宽容,这种类型的DNA修复可以帮助我们设计更安全、更高效的基因疗法”。
一种新的方式来纠正致病突变
标准基因治疗策略,依赖注入一个纠正的DNA作为模板修复突变参与这一过程被称为homology-directed修复(HDR)。
“HDR-based策略仍然遭受低效率和携带不必要的供体DNA整合的风险在整个基因组,”冯解释道。“国际卫生条例有可能克服这些问题,因为它依赖于自然细胞通路和病人的正常染色体校正的有害突变。”
冯的团队继续识别额外的DNA repair-associated蛋白质,可以刺激国际卫生条例,其中包括一些,不仅促进高水平的国际卫生条例,但也抑制DNA修复过程中的错误。额外的实验,允许团队研究的基因组特征国际卫生条例事件给了更深的洞察国际卫生条例的机制和方法建议的技术可以用来使基因疗法更加安全。
“尽管仍有很多了解这个新的《国际卫生条例》的应用,我们的发现一种新的基因治疗方法的基础,可以帮助解决一些大问题与当前的方法,“Aida说。
进一步探索
这个故事是由麻省理工学院新闻(再版web.mit.edu/newsoffice/),一个受欢迎的网站,包括麻省理工学院新闻研究、创新和教学。