一种现有的药物可能会将肿瘤相关的巨噬细胞变回癌症战士

一种被称为刺猬信号的细胞通信形式对哺乳动物的胚胎发育至关重要。但在包括乳腺癌在内的多种癌症类型中,异常激活的hedgehog信号会促进肿瘤侵袭,扩散到其他器官和多药耐药性。
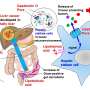
两年前,Lalita Shevde博士及其同事表明,刺猬信号在改变人体免疫成分中起着重要作用肿瘤微环境.现在他们报道了肿瘤相关巨噬细胞异常的hedgehog信号免疫细胞这应该是促进炎症的守护者肿瘤的生长-而是将它们转化为非侵袭性的免疫抑制巨噬细胞,称为M2巨噬细胞。
肿瘤微环境发出的这种信号表明,使用现有的、临床批准的刺猬信号抑制剂可能会降低肿瘤微环境中肿瘤相关M2巨噬细胞的促肿瘤特性。免疫抑制、交替极化M2巨噬细胞浸润升高与癌症患者预后不良有关。
阿拉巴马大学伯明翰分校的病理学教授Shevde在杂志上发表了她的研究,她说:“靶向hedgehog信号的吸引力来自于几种美国食品和药物管理局批准的抑制剂已经在临床使用,使其适用于不同类型的肿瘤。癌症研究.“我们的工作支持了这样一种可能性,即hedgehog基因阻断在重新校准代谢方面的作用是多方面的,因此,免疫抑制巨噬细胞的功能也是如此。
“因此,抑制hedgehog信号可能具有直接靶向的双重好处肿瘤细胞并将肿瘤免疫微环境重新配置为免疫激活状态。”
M1和M2巨噬细胞具有不同的代谢回路,有助于它们的生存和不同的免疫反应功能。M1巨噬细胞通过糖酵解代谢产生能量,这足以满足它们的肿瘤根除功能,而M2巨噬细胞则使用氧化磷酸化这是一种更有效的方式来产生促进肿瘤功能所需的能量。
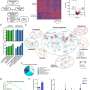
使用两个小鼠乳腺肿瘤模型,并用刺猬抑制剂Vismodegib治疗它们,Shevde和同事发现肿瘤浸润巨噬细胞发生了显著变化。该抑制剂显著改变了巨噬细胞的代谢,特别是减少了尿二磷酸n -乙酰葡萄糖胺生物合成途径的流量。
反过来,这对转录因子STAT6有下游影响,减少其O-linked-N-acetylglucosaminylation (O-GlcNAc)修饰,使其更活跃,这导致基因Arg1和Cd206的表达增加,这对M2巨噬细胞的免疫抑制状态至关重要。上调的STAT6活性也导致基因表达增加,将代谢转移到脂肪酸氧化用于代谢需求的M2巨噬细胞。
然而,当hedgehog抑制剂导致STAT6的o - glcnac修饰减少时,巨噬细胞的代谢和生物能学从氧化磷酸化和脂肪酸氧化转变为糖酵解。线粒体——细胞的能量来源——从典型的利用脂肪酸氧化的细胞融合的线粒体变成了碎片化的线粒体。
“这些刺猬抑制的巨噬细胞让人联想到炎性M1巨噬细胞,表型特征为碎片化的线粒体,”Shevde说。“这是第一次证明刺猬活性可以调节代谢和生物能量编程肿瘤相关巨噬细胞。此外,我们的工作为调节hedgehog基因活性以及巨噬细胞代谢提供了证据,从而塑造巨噬细胞的可塑性。”
刺猬信号包括所谓的刺猬蛋白,它们与细胞结合并在细胞内启动信号。该信号通路在胚胎发生过程中指导所有双侧动物的发育。最初的两个刺猬基因是从果蝇的突变中发现的,它们使果蝇幼虫看起来像刺猬一样短粗而尖锐,所以它们以刺猬的物种命名:沙漠刺猬和印度刺猬刺猬.第三个突变使苍蝇看起来像电子游戏角色刺猬索尼克,所以索尼克刺猬成为该基因的名字。
进一步探索