蛋白质,战胜新出现和重新出现的病毒
最出名的一个家庭的蛋白质作用在减少艾滋病毒传染性可能货物战胜其他新出现和重新出现的病毒,科学家们发现。
他们新发现的关键力量:增强信号免疫细胞释放的一个最强大的战士天生的抗病毒反应,蛋白质被称为I型干扰素。
细胞培养实验显示,这些蛋白质的信号活动,从SERINC家庭,帮助保护细胞从感染HIV,埃博拉病毒和Zika病毒病毒。研究人员目前正在对SARS-CoV-2测试这个函数是否还有效,导致COVID-19的病毒。
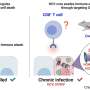
它的一件事蛋白质对一个特定的病毒直接作用,像SERINC5已被证明,通过融合成为艾滋病毒粒子在病毒生产。但这是另一件事完全揭示蛋白质具有增强作用必不可少的抗病毒细胞信号通路在感染宿主细胞后,高级研究作者Shan-Lu Liu表示的病毒学教授在俄亥俄州立大学兽医生物科学。
“病毒可以绕过直接抗病毒作用,”刘说,也是一个侦探和俄亥俄州的逆转录病毒研究中心副主任。“但如果这种蛋白质还可以调节关键通路没有代理直接在病毒,然后病毒可能有限的能力来应对它。
“如果这个家庭的分子可以在动物和人类,那么你可能会认为是否可以用于广泛的抗病毒疗法”。
今天的研究发表在《华尔街日报》(2021年9月14日)科学的信号。
刘了他所谓的“进化军备竞赛”艾滋病毒和人体免疫系统多年来,和领导一个2019研究描述了艾滋病毒蛋白质Nef基因可以占上风,fight-specifically通过干扰SERINC病毒制造细胞的蛋白质。
在这项研究中,刘和他的同事们仔细看看SERINC5功能在目标细胞在接下来的病毒感染阶段。他们发现,除了提高信号产生I型干扰素,SERINC5具有相同的信号,影响生成另一个组件的早期抗病毒response-NF-kB炎性细胞因子。
SERINC5不调节这个信号系统在其星体与其他蛋白质称为小牛和TRAF6加入部队。但它的一些具体行为仍然是一个谜,刘说。
在细胞培养病毒感染已经启动,研究人员发现SERINC5凡从细胞表面在线粒体外膜细胞的权力center-an不同寻常的举动。一旦,SERINC5与小牛和TRAF6形成一个多层面的复杂可能解释为什么它的作用是如此有影响力的信号通路中接下来会发生什么。
“这些蛋白质的聚合意味着他们需要对方以及这是一个令人激动的发现,”刘说,病毒病原体和新兴项目的主任在俄亥俄州立大学的传染病研究所。”这样的大型复杂可以招募额外的分子,提高信号转导通路的效率。”
这些招募分子是一连串的消息,导致I型干扰素生产和NF-kB炎性细胞因子从病毒感染细胞,发挥着至关重要的作用在限制病毒感染早期阶段。在实验中利用多种类型的人类和动物细胞培养,这种机制抑制受艾滋病毒感染的细胞,埃博拉病毒和Zika病毒。
相反,当细胞被修改了,所以他们没有产生SERINC5蛋白质,这些病毒在细胞复制more-suggesting SERINC多么重要的角色在这个过程中,强化的主要宿主细胞的抗病毒反应。
这项工作是在两个SERINC家族的成员,SERINC3 SERINC5,但刘推测其他版本可能有类似的效果。但仍有很多学习这些是什么触发SERINC5搬迁本身的细胞表面线粒体,它正常的细胞功能是当没有病毒。
至于是否可以抑制COVID-19病毒蛋白质的功能,刘持乐观态度。
“我的猜测是SERINC蛋白质会产生影响,因为我们知道I型干扰素对控制非常重要病毒在早期阶段,这种分子可以提高I型干扰素反应,”他说。“发现一种蛋白质,可以调节的关键途径,具有广泛的抗病毒effect-well,你可以想象这种蛋白质有一个广泛的抗病毒功能。”
更多信息:SERINC蛋白质加强抗病毒I型干扰素生产和炎性信号通路、科学的信号(2021)。www.science.org/doi/10.1126/scisignal.abc7611