当你的身体不能识别自己的左撇子RNA
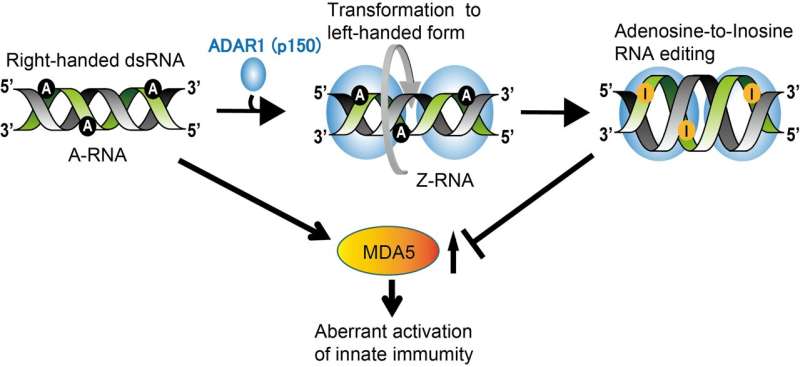
像DNA一样,RNA分子包含的信息通过四个不同的核苷酸的独特组合。分子称为RNA编辑的过程,然而,通过化学变化可以使腺苷核苷酸,将它们转换为一个叫做肌苷的酶称为核苷酸腺苷脱氨酶(亚)。ADAR-mediated RNA修改是必要的为了生存和两个阿达尔月,ADAR1 ADAR2,已确定在哺乳动物。在最近发表的一篇文章免疫力大阪大学学习,一群老鼠包含特定突变ADAR1,发现缺陷突变体酶RNA绑定导致异常生长和发展的老鼠。
两个版本的ADAR1蛋白质存在于老鼠细胞:p110 p150。先前的研究表明,ADAR1编辑双链RNA(极),这样细胞传感器叫做MDA5承认它正确地为“自我”RNA病毒RNA,没有错误(这将导致MDA5诱导免疫反应)。有趣的是,ADAR1 p150酶包含一个特定的绑定域名称为Z-RNA的特殊类型的RNA。双链RNA通常形成一个右手螺旋结构但Z-RNA dsRNA,左撇子的结构形式。
“突变ADAR1 p150,包括域内承认Z-RNA,与遗传有关炎症性疾病被称为Aicardi-Goutieres综合症(AGS),”说,该研究的第一作者Taisuke Nakahama。“我们想检查这个生物功能如何影响AGS发病机制。”
调查,团队生成转基因实验室老鼠点突变在这两个等位基因的基因编码ADAR1 p150。这种突变突变ADAR1废除Z-RNA绑定能力。突变小鼠显示严重抑制经济增长相对于野生型小鼠(non-mutant)。
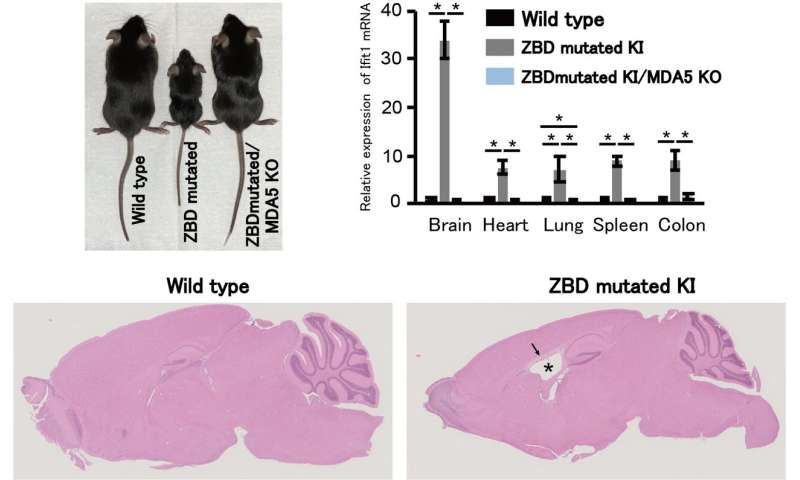
“基因突变小鼠异常发达的器官,包括关键的大脑,脾、和结肠,“日本资深作者Kawahara解释道。“迷人地,他们的畸形的大脑显示特征类似于脑病中观察到人类AGS的病人。”
突变体老鼠也显示干扰素刺激基因表达水平高,导致慢性炎症状态。通过额外的机械的实验中,团队证明ADAR1 p150 Z-binding域是至关重要的适当的RNA编辑由这种酶催化的。
“我们的研究表明,这一领域的交互与Z-RNA阻止免疫系统的一个关键第一步相信这个分子是一个外来入侵者,“Nakahama解释道。
本研究确定了不当Z-RNA AGS发病机理识别作为一个贡献者。这些发现将有助于发展新的治疗方法治疗这种疾病,也可以帮助我们进一步理解反应像SARS-CoV-2 RNA病毒的感染。