涉及心脏发育的蛋白质增强了干细胞策略以进行心脏修复
随着年龄的增长,人的心脏逐渐失去了受伤后修复自身的能力。因心脏缺血和心脏病发作而造成的损害与心脏中的氧气水平降低有关,可能导致心脏的功能低于正常能力,从而使患者难以进行日常活动。
为了增加缺血性损伤后的心脏修复,研究人员转向基于干细胞的疗法,这些疗法用新的功能组织代替死心组织。然而,在大多数情况下,不到1%的干细胞存活到心脏,这主要是由于细胞无法应付缺血性环境的代谢需求。
现在,在新的研究中,坦普尔大学刘易斯·卡茨医学院的科学家表明,至少在老鼠中,可以通过重新引入Lin28(通常在发育中的心脏中表达的蛋白质)来克服这一障碍,这是从发育中的干细胞中得出的。成人心脏组织。LIN28使成人心脏干细胞更具代谢柔性,从而大大提高了其生存机会。
刘易斯·卡茨医学院的心血管研究中心兼新的新的新型研究员的心血管研究中心的心血管科学助理教授Mohsin Khan博士解释说:“ Lin28非常活跃,但在成人心脏中却不活跃。”学习。“我们发现,当我们在成人心脏组织的心脏干细胞中表达LIN28时,对成年细胞进行了重编程以具有年轻,发育中心细胞的代谢特征。该过程实际上就像反向衰老一样。”
新发现已在线发布在《期刊》上氧化还原生物学。
胎儿心脏特别适应低氧条件下的功能。在产后,这种低氧耐受性却丧失了,成年后,心脏对氧气可利用率的降低非常敏感。细胞代谢的变化是这种转变的根本原因,最近的研究表明,心脏中的这些代谢差异有助于确定移植后干细胞的命运。
在新的研究中,Khan博士及其同事有兴趣发现在发育中心表达的代谢调节剂是否可以赋予心脏组织衍生的类样干细胞(CTSC)的代谢灵活性。CTSC存在于新生儿和成人心脏组织中,但仅在发育中的心脏中表达LIN28。在成人心脏组织中,CTSC具有再生潜力,通常处于休眠状态。
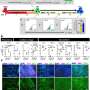
该团队首先在体外重新引入了成年小鼠CTSC中的LIN28表达,并分析了对细胞代谢,生长和再生所涉及的信号通路的影响。他们发现LIN28表达产生了鲁棒的再生反应,从而改变了CTSC,以促进氧化应激的生长和存活。研究人员将修饰与LET7/PDK1信号通路联系起来,该途径已知可以调节细胞中的有氧代谢。在遭受的小鼠中,将表达LIN28的CTSC移植到心脏中心脏病发作导致心脏结构和功能显着改善。这些作用是通过体外评估中鉴定出的相同途径介导的。
Khan博士解释说:“ LIN28在CTSC中修改了能源生产,导致了许多对心脏细胞存活有益的因素的分泌。”“总的来说,细胞进行了更年轻的表型。”
Khan博士计划将新发现转化为更大的动物模型,并确定人类衍生的心脏干细胞可以通过LIN28重新编程。“这些研究可能对我们如何处理干细胞疗法具有重要意义心人类疾病。”他说。