研究表明为什么免疫检查点封锁阻碍但不停止胶质母细胞瘤进展
像锁门,但打开窗户,免疫疗法检查站暂时放缓胶质母细胞瘤(GBM)进展但未能建立有效的抗肿瘤微环境和似乎增加分子相互作用抑制长期免疫反应,根据加州大学洛杉矶分校的一个研究小组研究了。
在11月26日的问题自然通讯,研究人员解释为什么PD-1 blockade-which对其他人士有效的针对这些不足致命的脑瘤。他们还提供免疫景观细节和提出未来战略和调查。
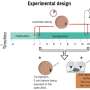
“原发性脑瘤,胶质母细胞瘤等,非常抗免疫疗法。在临床前研究中,免疫疗法似乎是有效的,在以前,小,1期临床试验使用anti-PD-1疗法tumor-removal手术之前,是干扰素诱导的生存和长度增加。但治疗不治疗,表明还有其他微环境中的相互作用,这种治疗没有地址,”主要作者罗伯特·m·普林斯说,博士,加州大学洛杉矶分校的研究员Jonsson综合癌症中心肿瘤免疫学家和加州大学洛杉矶分校的大卫格芬医学院的教授。
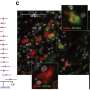
识别的几种机制和交互的有限的成功和最终失败负责PD-1封锁阻止大脑肿瘤恶化,王子与威利雨果博士和其他来自加州大学洛杉矶分校Jonsson综合癌症中心的同事,加州大学洛杉矶分校的多个部门的健康,帕克癌症研究所免疫疗法在旧金山在单细胞分析免疫细胞的数量与先进的单细胞技术水平。
PD-1,所谓“蛋白质检查站”,帮助T细胞从正常免疫系统调节的攻击,正常的作为一个“开关”保护正常细胞。然而,许多癌症劫持过程来保护自己免受攻击。在肺、皮肤和其他癌症,单克隆抗体抑制政府检查站蛋白使T细胞恢复攻击癌症细胞。
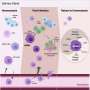
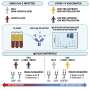
在胶质母细胞瘤中,研究人员发现,PD-1封锁最初增加的比例和数量的一个子集“祖筋疲力尽”T细胞激活传统人口的树突细胞,但免疫微环境仍主要由其他免疫细胞(骨髓细胞)产生炎症分子和免疫抑制。要有效,PD-1封锁可能需要结合疗法针对其他检查点蛋白和免疫抑制途径。
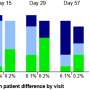
根据作者,结果表明anti-PD-1治疗最初激活T细胞在血液中,其中一些迁移到肿瘤微环境和生产干扰素γ。
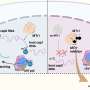
尽管积极anti-PD-1治疗的早期影响,人口的白血细胞(单核细胞和巨噬细胞)招募到肿瘤微环境似乎也应对干扰素信号不适应的方式。Anti-PD-1疗法似乎增加这些细胞之间的相互作用和另外两个检查站在T细胞表达下调免疫反应,CTLA-4 TIGIT。
这些交互可能限制抗肿瘤的大小和持久性T细胞活动,普林斯和雨果说。数据显示,anti-PD-1治疗改善生存结果通过增加抗肿瘤T细胞反应,但治疗也改变肿瘤微环境和影响non-T细胞群。的有效性的第一反应是减少额外的T细胞的接触检查点,也和新的战略目标其他免疫抑制通路可能提高反的强度和耐久性肿瘤响应。
更多信息:亚历山大·h·李等新辅助PD-1封锁诱发T细胞和cDC1激活但未能克服免疫抑制肿瘤相关巨噬细胞在复发胶质母细胞瘤,自然通讯(2021)。DOI: 10.1038 / s41467 - 021 - 26940 - 2