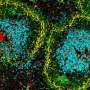
隐形的方式对抗肿瘤
在适当的情况下,身体的T细胞可以检测和摧毁癌细胞。然而,在大多数癌症患者,T细胞成为解除武装,一旦他们进入肿瘤周围的环境。
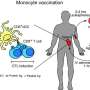
科学家们正在试图寻找方法来帮助治疗病人通过重启那些黯淡的T细胞。为这一领域的研究,被称为癌症免疫疗法,都集中在寻找刺激这些T细胞直接。麻省理工学院的研究人员已经发现了一个可能的新方法间接激活T细胞,通过招募人口的助手称为树突状细胞的免疫细胞。
在一项新的研究中,研究人员发现了一个特定子集的树突细胞有激活T细胞的独特方式。这些树突细胞可以斗篷肿瘤蛋白质,让他们模仿癌细胞,引发强烈的T细胞反应。
“我们知道树突细胞抗肿瘤是非常重要的免疫反应,但是我们不知道真正构成最优树突细胞响应肿瘤,”霍华德Stefani突然说美国麻省理工学院的教授和琳达·b·斯特恩的职业发展和麻省理工学院的一个成员的科赫研究所综合癌症研究。
结果表明,寻找刺激,特定人口的树突细胞可以帮助提高癌症免疫疗法的有效性,她说。在老鼠的一项研究中,研究人员表明,刺激这些树突细胞黑色素瘤的生长速度减缓和结肠肿瘤。
跳是这项研究的资深作者,今天出现在杂志上免疫力。论文的第一作者是麻省理工学院研究生艾伦Duong。
自然的回归
肿瘤开始形成时,产生T细胞癌蛋白质识别作为外交。这有时使T细胞消除肿瘤之前非常大。在其他情况下,肿瘤能够分泌化学信号,取消激活T细胞,使肿瘤继续无节制的增长。
树突细胞来帮助激活攻击T细胞,但有许多不同亚型的树突细胞,T细胞激活和各自的角色不是完全的特征。在这项研究中,麻省理工学院的团队想要调查哪些类型的树突细胞参与T细胞反应,成功地消除肿瘤。
要做到这一点,他们发现一个肿瘤细胞系,从肌肉类型的肿瘤,这已被证明在小鼠自发地回归。这样的细胞系是很难找到,因为研究人员通常不让他们如果他们不能形成肿瘤,突然说。
对小鼠的研究中,他们比较肿瘤产生的退化的细胞与一种结肠癌癌,形成肿瘤长大后被植入人体。研究人员发现,在肿瘤进展,T细胞反应很快就筋疲力尽,在回归肿瘤,T细胞功能。
之后,研究人员分析了树突状细胞数量,出现在每一个肿瘤。树突细胞的主要功能之一就是从垂死的细胞碎片,如肿瘤细胞或细胞感染病原体,然后现在的T细胞的蛋白质片段,提醒他们感染或肿瘤。
最著名的所需类型的树突细胞抗肿瘤免疫力是DC1细胞,这与T细胞能够消除癌症细胞。然而,研究人员发现,DC1细胞不需要肿瘤回归。利用RNA单细胞测序技术,相反,他们发现了一种以前未知的DC2细胞活化状态,不同类型的树突细胞,这是驾驶T细胞激活的回归肿瘤。
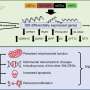
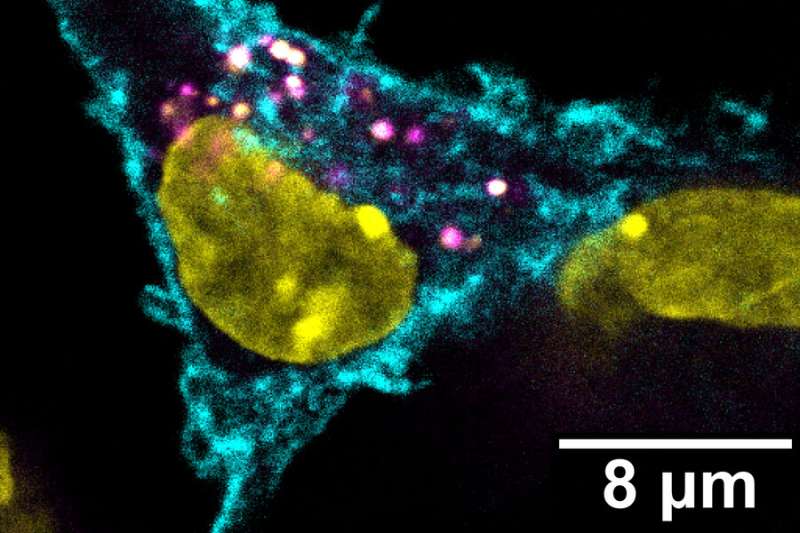
麻省理工学院的研究小组发现,而不是摄入细胞碎片,这些树突细胞从肿瘤细胞叫做MHC刷卡蛋白质复合物,并将它们显示在自己的表面。当T细胞遇到这些伪装成肿瘤细胞的树突细胞,T细胞变得强烈激活并开始杀死肿瘤细胞。
这个特殊人群的树突细胞似乎是由1型干扰素,激活细胞信号分子,通常产生针对病毒感染。研究人员发现一个小的人口这些树突细胞在结肠癌和黑色素瘤肿瘤进展,但是他们没有被正确地激活。然而,如果他们与干扰素治疗这些肿瘤树突细胞开始刺激T细胞攻击肿瘤细胞。
靶向治疗
某些类型的干扰素被用来帮助治疗癌症,但它有普遍的副作用,当给定的系统。来自本研究的发现表明,它可能是有利于实现干扰素在靶向肿瘤细胞的方法,或使用一种药物,引起肿瘤细胞产生的I型干扰素,突然说。
研究人员现在计划研究需要多大的I型干扰素产生强大的T细胞反应。大多数肿瘤细胞产生少量的I型干扰素但不足以激活能刺激T细胞的树突细胞群。另一方面,太多的干扰素可以对细胞毒性。
“我们的免疫系统是天生对微妙的I型干扰素的差异非常显著,这是有趣的从免疫学的角度来看,“突然说。
更多信息:蒂芬妮跳,i型干扰素激活MHC-I-dressed CD11b +传统树突状细胞促进保护抗肿瘤CD8 + T细胞免疫力,免疫力(2021)。DOI: 10.1016 / j.immuni.2021.10.020。www.cell.com/immunity/fulltext…1074 - 7613 (21) 00458 - 1