改善结肠直肠癌患者的药物选择

大肠癌患者是第一批接受靶向治疗的患者。这些药物的目的是阻断引发细胞生长失控的致癌蛋白质,同时保护健康组织。但一些患者不适合这些治疗,因为他们有促癌突变,据信这些突变会导致对这些药物的耐药性。
现在,索尔克大学助理教授、内科科学家爱德华·斯蒂茨(Edward Stites)利用计算机建模和细胞研究来发现更多病人一种普通的靶向疗法可能会比之前认为的有所帮助。研究结果于2021年12月14日发表细胞的报道.
“结直肠癌症那些已经尝试了所有标准治疗方案但癌症仍在进展的患者需要新的治疗方案。我们的研究表明,一种已经可用的靶向疗法每年可以使多达12000名额外的结肠癌患者受益,”该论文的资深作者Stites说。“我们的发现是临床前的,我们希望这项研究能激励临床医生开展临床试验,进一步检验我们的结果。”
Stites对研究靶向一种叫做EGFR(表皮生长因子受体)的蛋白质的药物很感兴趣。已知表皮生长因子受体会导致一些不同类型的癌症,包括肺癌和肺癌结肠直肠癌.
2004年,美国食品和药物管理局(FDA)首次批准了西妥昔单抗药物阻断结直肠癌中的EGFR活性从那时起,其他靶向EGFR的药物也获得了批准。但从这些药物的早期开发来看,医生们认为,在RAS蛋白家族中的任何一种发生突变的患者都不会对EGFR药物产生反应。因此,每当患者的肿瘤分子检测显示RAS突变时,患者就不会接受这些靶向治疗。
早期的研究并不是所有的RAS基因都是如此突变以同样的方式行事,并能够解释一个众所周知的,但很少被理解的规则例外。在这项新研究中,研究小组将计算和实验方法结合起来,使用这一新的解释来发现更多不应该导致对EGFR药物耐药的RAS突变。
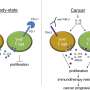
研究人员使用了除了特定RAS突变外完全相同的癌症细胞。这使他们能够比较每种特定的突变如何影响对egfr抑制药物的反应。他们发现,一些RAS基因突变并不会阻止药物发挥作用。这些实验也使他们能够验证他们的计算研究,这有助于确定新的计算方法如何有助于改善癌症患者的治疗方案。
研究人员还检查了不同的RAS突变体与另一种称为NF1的蛋白质的结合情况。Stites之前的数学模型暗示NF1可能在细胞对靶向药物的反应中发挥关键作用。在他们的新研究中,他们揭示了不能很好地结合NF1的RAS突变体对EGFR药物保持敏感性,而能很好地结合NF1的RAS突变体对EGFR药物具有耐药性。这种与EGFR药物的关系最初并不明显,但计算建模能够从可用的和不同的数据中发现它。
最终,研究人员确定了10种不同的RAS突变,不排除使用EGFR抑制剂。许多对这些突变有效的药物已经被FDA批准用于其他用途,这意味着医生甚至可以在临床试验进行之前就开始“非标签”地为患者开处方。
担任赫斯特基金会发展主席的Stites强调,这项研究也有助于验证他的团队开发的数学和计算方法。“模型可以解决传统方法无法解决的科学问题,”他说。“我们希望这样的未来临床试验将有助于确定益处的大小,以及我们确定的所有RAS突变是否对egfr抑制药物同样敏感,以及RAS之外的其他突变如何影响反应的强度。”
这篇论文的第一作者是托马斯·麦克福尔(Thomas McFall),他曾是索尔克大学的博士后,现在就职于威斯康星医学院。