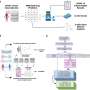
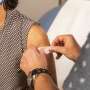
欧盟将返回该公司COVID疫苗
欧盟药品监管机构周一将决定是否批准COVID注射诺瓦瓦克斯公司,它使用一个更传统的技术,美国生物技术公司希望将减少疫苗踌躇。
诺瓦瓦克斯公司的疫苗、蛋白质疫苗全世界的使用防止许多儿童期疾病,将第五冠状病毒对欧盟授权。
马里兰批准也会促进公司的疫苗一直饱受延误。
欧洲药品局(EMA)表示,其人类药物委员会将举行特别会议来决定该公司周一,和“将沟通结果”。
欧盟已经签署了一项协议购买2亿剂疫苗的双人特写镜头等待总部位于阿姆斯特丹监管机构的批准。
该公司表示,其疫苗显示,90.4%功效对COVID-19北美的审判。
首席执行官斯坦利Erck说该公司“期待提供额外的疫苗在欧洲,选择建立在证明,易于理解技术平台”。
疫苗”可以帮助解决全球疫苗接种的主要障碍,包括全球分销和挑战疫苗犹豫”,Erck补充道。
在教学身体的所有疫苗工作免疫系统冠状病毒攻击,但他们以不同的方式做这件事。
诺瓦瓦克斯公司所谓的蛋白亚基技术已经尝试和测试,已经使用了几十年接种人对抗疾病,包括乙型肝炎和百日咳。
这也意味着它不需要存储在极低的温度,可能物流优势其他疫苗。
的生产问题
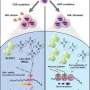
诺瓦瓦克斯公司利用微小,实验室的碎片蛋白质表面的冠状病毒。
当注入,这些引发免疫系统的反应,所以如果以后接触COVID病毒,它知道攻击它。
相比之下,Pfizer-BioNTech和现代化的疫苗一直主导着全球COVID反应使用开创性,但迄今为止很大程度上未经验证的信使核糖核酸(mRNA)技术。
他们使用一个称为遗传物质RNA分子带个口信给细胞产生的蛋白质。人体的免疫系统然后学会识别蛋白质和攻击。
病毒载体的方法使用阿斯利康和强生(Johnson & Johnson)的作品在一个类似的原则,但是传递遗传信息通过一个版本的感冒腺病毒作为一个“向量”。
罕见但严重的副作用的心脏炎症与信使核糖核酸疫苗已报告,并与病毒载体疫苗血凝块。
但是该公司一直与月的延迟在一群议员最近所谓的“生产问题”。
印度尼西亚和菲律宾已经批准该公司注射,而日本已同意购买1.5亿剂。
该公司说,它还申请批准在英国,印度,澳大利亚,新西兰,加拿大,和世界卫生组织。
该公司还表示,它正在“评估其疫苗ο变体”,致力于一个Omicron-specific版本。
©2021法新社