研究人员绘制了与阿尔茨海默病相关的糖基化模式
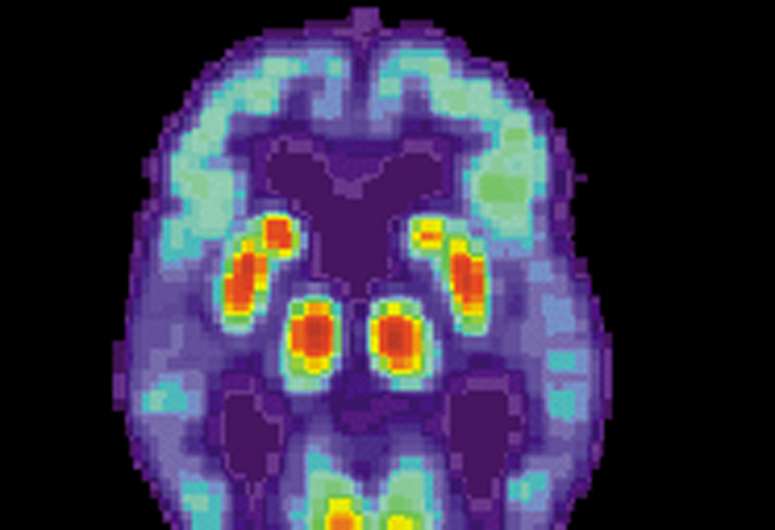
肯塔基大学的研究人员使用新的方法绘制了来自已故健康个体或阿尔茨海默病患者的大脑蛋白质上附着的糖链的变化。
到目前为止,还没有有效的治疗阿尔茨海默病(AD)的方法。迫切需要新的方法来预防这种毁灭性的神经系统疾病的发展。
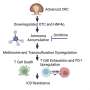
英国医学院神经科学助理教授、马基癌症中心研究员Ramon Sun博士和英国医学院分子和细胞生物化学教授、拉福拉癫痫治疗计划主任Matthew Gentry博士的实验室开发了一种新的成像方法来识别癫痫的特定模式糖附在组织内蛋白质上的分子。他们研究的糖附着的形式被称为n -糖基化。他们应用这种方法分析了两只AD小鼠模型和死于痴呆症的个体大脑中的“糖代码”。
他们研究的小鼠模型代表了AD患者常见的两种不同的病理。一种是老鼠积累蛋白质β(β淀粉样蛋白)在大脑;在另一个实验中,小鼠大脑中积累了异常形式的tau蛋白。尽管有不同的潜在病理,但两种小鼠模型在额叶皮层和海马体中都表现出增加的n -糖基化。
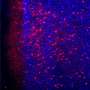
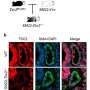
他们还分析了三名年龄匹配的个体和三名a β型阿尔茨海默病患者的大脑样本。和老鼠的大脑一样,阿尔茨海默病患者大脑额叶皮层的糖基化也增加了。然而,与在小鼠中观察到的相反,AD患者的海马区n -糖基化减少。
研究结果确定了AD患者额叶皮层和海马体的区域特异性差异。具体地说,n -糖基化增加的区域观察到额叶皮质海马区n -糖基化降低。此外,这项研究强调了AD小鼠模型和人类患者海马区n -连接蛋白糖基化模式的根本差异。
“这项研究可能有助于发展新的研究方向,新的治疗靶点,以及未来治疗和诊断AD的生物标志物评估,”孙说。这项工作最近发表在阿尔茨海默氏症阿兹海默症协会(Alzheimer's Association)的杂志。
Sun和Gentry及其团队在《内分泌学与代谢趋势》(Trends in Endocrinology & Metabolism)上发表了一篇综述,探讨了理解n -糖基化模式和大脑中这一生化过程的调节的重要性。n -连接蛋白的生物合成糖链是葡萄糖代谢的一个有待研究的分支。在细胞内,葡萄糖可以用于能源生产或者构建复杂的糖链来修饰蛋白质或脂质。这些过程争夺细胞中有限的葡萄糖来源。
“在中枢神经系统中,n连接蛋白糖基化对神经元和神经胶质细胞都至关重要,”医学院博士生、该手稿的主要作者塔拉·霍金森(Tara Hawkinson)说。这一过程控制了参与神经元活动的关键蛋白质的许多方面。糖基化异常可导致神经元功能障碍和死亡。
因此,改变的蛋白质糖基化可导致各种类型的神经元疾病,从与神经元损失相关的疾病,如阿尔茨海默病和帕金森病,到与神经元连接缺陷相关的疾病,如精神分裂症和发育性神经障碍。
由Sun和Gentry实验室开发的用于评估大脑中n -糖基化模式的糖编码空间分布的方法将使研究人员能够提出关于这些模式在病理条件下如何改变的关键问题。
金特里说:“有了这些方法学上的进步,我们可以开始回答脑细胞如何协调葡萄糖代谢来平衡能量需求和糖基化需求,糖编码的改变如何导致神经系统疾病,并开始开发治疗方法来解决这些问题。”