帕金森氏病突变误导大脑中的铁
根据12月16日在开放式杂志上发布的一项新研究,帕金森氏病的常见基因突变驱动了激活的小胶质细胞中铁的错误定位。PLOS生物学,由美国国家老化和同事研究所的马克·库克森(Mark Cookson)。结果可能有助于解释疾病中受影响的大脑区域中有毒铁的积累,并为开发旨在纠正铁运输缺陷的疗法的发展提供了基础。
LRRK2基因中的突变约占所有家族性帕金森氏病的5%,约占非家庭疾病病例的1%。LRRK2是一种激酶,一种酶,通过添加磷酸盐和引起疾病的蛋白质来调节其他蛋白质突变已知会增加酶的激酶活性。LRRK2调节的靶标之一称为Rab8a,一种蛋白质与RAB家族的许多其他蛋白质一起,有助于控制各种细胞囊泡(膜结合的亚细胞隔室)的运动或“运输”。RAB8A的工作之一是通过转铁蛋白受体调节铁进口到细胞,并在释放转铁蛋白及其携带的铁后帮助将该受体回收回膜。
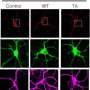
为了了解帕金森氏病中发现的LRRK2突变如何影响这一过程,作者首先可视化了含有致病突变的LRRK2小鼠星形胶质细胞中的Rab8a运动。他们发现突变蛋白负责将RAB8A从内吞回收室的正常位置重定向,并在受损的溶酶体处进行隔离。
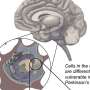
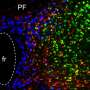
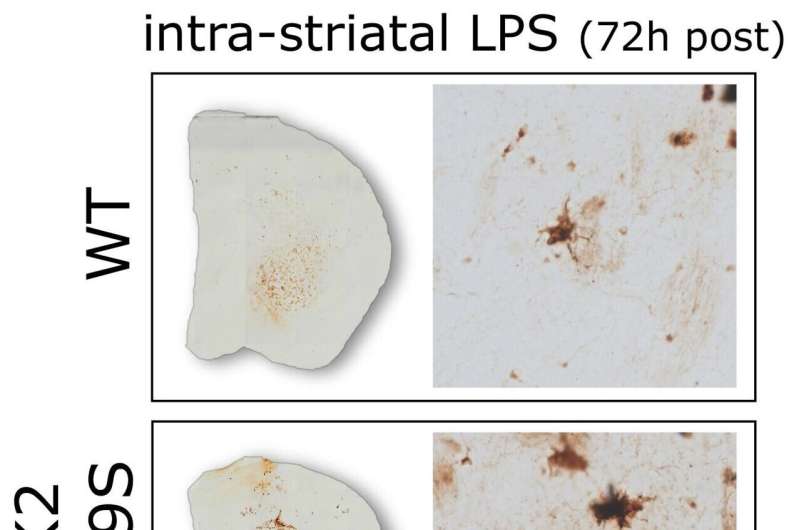
RAB8A的这种错误定位对转铁蛋白受体有明显的影响:在含有正常LRRK2的细胞中,转铁蛋白受体分布在多种囊泡类型之间。然而,在包含帕金森突变体LRRK2的细胞中,转铁蛋白受体及其铁聚集在发现Rab8a和突变体LRRK2的同一受损溶酶体上。在源自源自的活化的小胶质细胞中观察到了Rab8a和转铁蛋白受体的错误定位人类细胞携带致病性LRRK2突变。小胶质细胞是大脑炎症的关键驱动因素。最后,当携带同一帕金森氏突变的小鼠暴露于促炎触发时,铁在纹状体中积聚在小胶质细胞中,纹状体是控制运动的大脑区域,是帕金森病中大脑中最突出的部分之一。
库克森说:“我们的数据表明,LRRK2帕金森氏病发病机理的关键步骤是蛋白质与RAB8A的相互作用及其随后对活化小胶质细胞中铁错误定位的影响。”大脑中的铁沉积是帕金森氏病和其他神经退行性疾病,其积累可能会驱动自由基生产和对线粒体的损害,这两者都被认为是疾病级联的关键步骤。“这些结果应有助于我们理解阻止LRRK2作为帕金森氏病的潜在治疗方法的含义。”
库克森补充说:“我们的研究表明,基于基因LRRK2的帕金森氏病模型中铁的调节改变了。”“以前的数据表明铁可以沉积在大脑中,我们现在与已知的帕金森氏遗传原因联系在一起疾病这可能与新型治疗有关。”
进一步探索