单细胞空间分析可能有助于预测三阴性乳腺癌对新辅助免疫治疗的反应

一项新一代技术允许研究单细胞水平的蛋白质表达和肿瘤微环境(TME)中的细胞位置是可行的,并提供了关于将免疫检查点抑制剂atezolizumab (Tecentriq)添加到化疗中作为早期高危和局部晚期三阴性乳腺癌(TNBC)患者的新辅助治疗的益处的信息圣安东尼奥乳腺癌研讨会2021年12月7日至10日举行。
米兰IRCCS Ospedale San Raffaele临床肿瘤科乳腺癌组主任、主讲人Giampaolo Bianchini医学博士说:“我们正在经历一场表征肿瘤分子复杂性的技术革命。”“其中,成像大规模细胞术使我们能够收集有关肿瘤及其周围微环境异质性的前所未有的信息。”
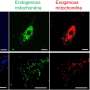
通过成像大规模细胞术(IMC),可以同时分析单个组织切片中的40多个标记物,以识别上存在的一组蛋白质单个细胞Bianchini解释说,这可以解释它们在组织中的精确位置。IMC结合流式细胞术原理,分析单个细胞或者当粒子流过单个或多个激光时,以及质谱法,通过精确测量样本中的分子质量来识别它们。
新出现的证据表明,TNBC肿瘤浸润单核细胞和淋巴细胞。在KEYNOTE-522试验中,联合免疫检查点抑制和化疗对高危TNBC患者有显著益处,导致FDA批准pembrolizumab (Keytruda)联合化疗作为这种情况下的新辅助治疗。
“不幸的是,一种方法并不适合所有患者,其中一些患者可能只对化疗有反应,而其他最初受益于免疫治疗的患者最终会复发。此外,尽管免疫疗法总体上耐受性良好,但一些罕见但潜在严重的免疫相关副作用已被报道,”Bianchini评论道。“由于这些原因,我们迫切需要生物标记物来帮助我们确定哪些患者将从免疫治疗中受益最大——可能导致化疗降级或无化疗策略,以及那些仅使用化疗就能恢复良好的患者。”
Bianchini和他的同事研究了IMC是否可以帮助确定这种治疗方法的理想候选。他们在III期的背景下进行了IMC分析NeoTRIPaPDL1该试验旨在评估将atezolizumab (Tecentriq)添加到卡铂和nab-紫杉醇(Abraxane)化疗中,与仅使用卡铂和nab-紫杉醇相比,作为早期高危和局部晚期TNBC患者的新辅助治疗,这些患者在治疗结束后6周内接受了手术。
“我们通过单细胞分析评估了识别肿瘤和TME中存在的不同表型的预测价值,以及细胞-细胞相互作用的相关性,”英国癌症研究所剑桥研究所和剑桥大学的小组负责人、该研究的主要贡献者H Raza Ali医学博士说。“细胞之间的物理相互作用是免疫激活和肿瘤细胞杀伤所必需的,因此在研究对免疫治疗的反应时,肿瘤组织的空间组织信息是至关重要的。”
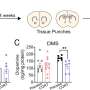
研究人员成功地分析了在100多万个单细胞中表达的43种蛋白质组织样本通过对243例患者(占研究人群的86.8%)进行治疗前活检收集。对于每个样本,他们生成了三个包含肿瘤、肿瘤-基质界面和相邻基质的高维图像。他们研究了肿瘤和TME细胞上的蛋白质表达、细胞表型以及与病理完全缓解率(pCR)的空间组织的关系,病理完全缓解率(pCR)定义为手术期间收集的组织样本中没有侵袭性癌细胞。
根据作者的说法,大块蛋白质表达分析可能提供有限的预测信息,因为它没有考虑每个蛋白质表达的细胞室。例如,在TME细胞上评估Ki67,在上皮细胞上评估HLA-DR,似乎比在整个组织标本中评估相同的生物标志物提供了更多的预测信息。
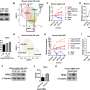
通过允许精确识别不同的细胞表型,包括细胞类型和功能状态,这种方法揭示了某些细胞群密度的潜在预测作用:在接受atezolizumab联合化疗的患者中,PD-L1和免疫抑制分子IDO高表达的抗原呈递细胞和CD56神经内分泌标志物高表达的上皮细胞的高密度与较高的pCR相关,而在仅接受化疗的患者中则没有。
此外,上皮细胞与特异性TME细胞之间高度的空间连通性,例如具有颗粒酶B或PD1表达的CD8+ T细胞和衰竭特征,与atezolizumab后pCR率的显著增加相关,而这些标志物的低表达与atezolizumab组和仅化疗组之间的pCR率相似相关。
Bianchini评论说:“我们的研究结果表明,TME中特定细胞之间相互作用的空间数据可能对免疫检查点抑制剂(如atezolizumab)在化疗之外提供的益处提供了非常丰富的信息。”“这种类型的信息只能通过允许我们同时精确地描述单细胞及其空间定位的技术来提供。”
该方法还证实了TNBC的极端异质性,无论是在肿瘤细胞组成方面,还是在数量、类型和功能状态方面细胞存在于TME中。
“我们通过IMC获得的预测信息补充了常用的免疫生物标志物,如PD-L1表达或间质肿瘤浸润淋巴细胞的数量。此外,我们发现一些捕捉免疫细胞类型和功能的免疫相关基因表达特征比IMC评估的相应生物标记物信息更少,”Bianchini说。
IMC技术的复杂性导致人们质疑它是否可以应用于大系列的肿瘤样本,例如在常规实践中收集的肿瘤样本。Bianchini补充说:“在我们的研究中,我们证明了这种颠覆性技术可以成功地应用于大型临床试验中前瞻性收集的样本,为其在癌症研究中的广泛应用铺平了道路,以帮助精确免疫学。”
根据作者的说法,这项研究的所有发现都需要独立验证。此外,没有采用多次比较的正式调整,因此需要谨慎地解释结果。最后,这项技术在研究环境之外的可重复性和适用性仍然必须进行调查。
更多信息:文摘:GS1-00。NeoTRIPaPDL1试验中三阴性乳腺癌(TNBC)的单细胞空间分析和免疫治疗反应