恶性血液病新治疗靶点确定
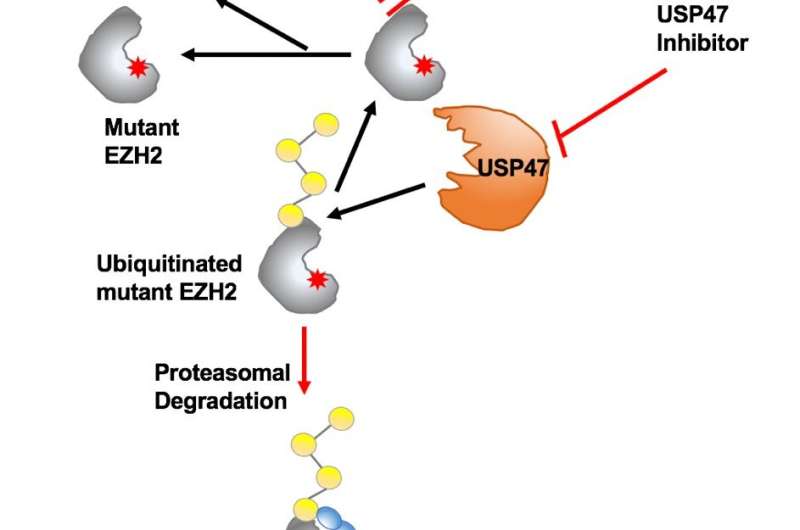
中国科学院合肥物质科学研究院的科学家表示,抑制泛素特异性肽酶47 (USP47)被确定为一种新的治疗靶点,用于治疗含有突变癌蛋白EZH2的恶性血液病。研究结果发表于白血病.
该研究的第一作者杨洁表示,这是一种去泛素化酶(DUB),可以选择性地稳定突变体EZH2。
恶性血液病是一种始于血液产生的骨髓的癌症。最近,表观遗传调控因子zeste同源物2增强子(Enhancer of zeste homolog 2, EZH2)由于其高频率突变,已成为弥漫性大b细胞淋巴瘤(DLBCL)和成人急性髓系白血病(AML)的关键靶点。然而,继发性突变和EZH2的酶活性独立作用引起耐药性酶抑制剂长期治疗后。因此,破坏突变EZH2蛋白可能更有效地靶向EZH2突变癌症和克服耐药性。
在这项研究中,使用化学遗传筛选并结合临床前模型研究,Yang和她的同事发现小分子化合物诱导泛素介导的突变EZH2降解,导致AML和DLBCL细胞在体外和体内死亡。
通过广泛的选择性分析,他们发现USP47是一种新的DUB稳定突变体EZH2,也是突变体EZH2阳性血液系统恶性肿瘤的潜在治疗靶点。
USP47在突变EZH2表达细胞中高度表达,与突变EZH2结合并稳定于wt EZH2。抑制USP47可使wt EZH2在正常细胞中存活,从而避免了临床治疗中的不良副作用。
他们发现USP10在AML中选择性靶向FLT3- itd和激酶抑制剂耐药性FLT3突变体,而JOSD1抑制剂在AML中选择性靶向JAK2-V617F。
“通过DUB促进突变体EZH2的降解来治疗性靶向抑制而不是抑制它酶活性是一种创新的方法,可能有助于克服对当前EZH2酶抑制剂的耐药性,”杨说。
“我们的发现提供了潜在的好处不良副作用来自哈佛医学院丹娜-法伯癌症研究所的共同第一作者Ellen Weisberg说:“这与EZH2抑制临床使用以及克服与EZH2激酶抑制相关的技术限制有关,这些限制会降低临床疗效。”