美国食品和药物管理局的审查员对新的渐冻症药物表示反对

尽管患者维权人士进行了数月的激烈游说,但联邦卫生官员周一公布了一种治疗肌萎缩性侧索硬化症(ALS)的实验性药物的基本负面评论。
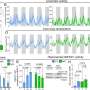
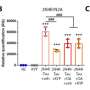
在对Amylyx制药公司的药物美国食品和药物管理局(fda)的监管人员表示,该研究结果“没有说服力”。他们指出了缺失的数据、招募患者的错误以及其他问题。与此同时,在一项137名患者的中期研究中,这种药物只是适度减缓了疾病的进展。FDA咨询委员会将于周三开会,考虑Amylyx的请求,即跳过通常需要的三期临床试验,并根据早期数据批准其药物。数十名渐冻症患者和倡导者计划在会议上发言,FDA将权衡小组的审议和投票,然后对该药物做出最终裁决,预计将于6月做出最终裁决。
AMX0035是由两种已知药物成分苯基丁酸钠和牛磺酸二醇组合而成。苯丁酸钠的品牌名为Buphenyl,用于治疗肝脏疾病,而牛磺酸二醇是一种膳食补充剂用于古代中医。一些渐冻症患者已经同时服用这两种药物。FDA的批准可能会迫使保险公司承担治疗费用。
直到去年年底,FDA还坚持要求Amylyx完成正在进行的三期临床试验,然后才能申请批准AMX0035。去年12月,fda做出了让步,开始对该药物申请进行优先审查,并将6月29日定为最终决定的目标日期。
ALS协会为Amylyx的研究投资了220万美元,这笔钱是在网上疯转的冰桶挑战活动中筹集的。ALS协会首席任务官尼尔·塔库尔博士告诉记者,作为投资的一部分,ALS协会拥有“少量特许权使用费股份”,如果该药物获得批准,将可获得高达330万美元的收益每日健康.他说,从AMX0035获得的任何资金都将投入到研究中。最终的希望就是这样药物开发在冰桶挑战资金的推动下,将会出现延长ALS患者生命的药物组合,直到找到治愈方法。
更多信息:FDA分析
©2022健康日。版权所有。