T细胞来源的白细胞介素-22如何促进结肠隐窝的抗菌防御
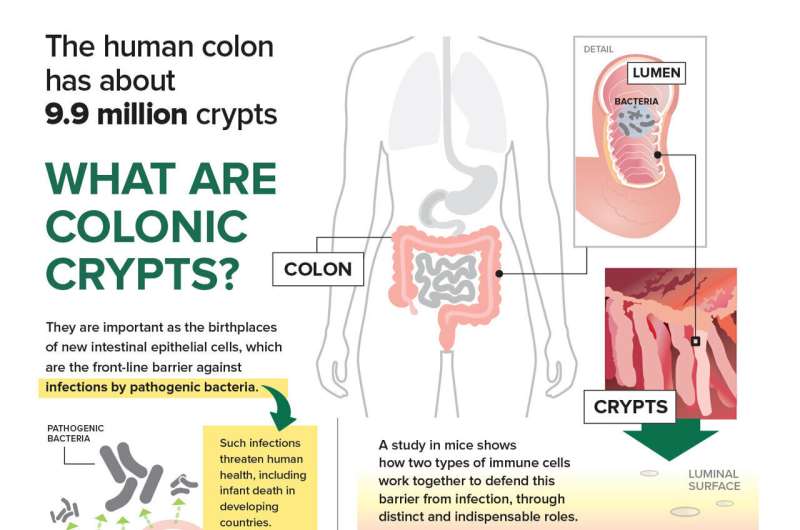
肠上皮细胞排列在肠道内壁,为肠致病性大肠杆菌等危险细菌创造了一道屏障,这些细菌试图附着并消除这道屏障,导致腹泻。这些病原体对人类健康构成重大风险,并在发展中国家造成婴儿死亡。
在该杂志上发表的一项研究中免疫力Carlene L. Zindl博士和Casey T. Weaver,医学博士,阿拉巴马大学伯明翰分校病理学系展示了两种类型的免疫细胞——一种是先天免疫系统的一部分,另一种是适应性免疫系统的一部分——如何发挥独特而不可或缺的作用来防御这种屏障。
韦弗说:“在这项研究中,我们定义了产生白细胞介素22的T细胞在结肠隐窝的抗菌防御中的非冗余作用。”“我们的发现解决了先天免疫和适应性免疫的协调以及先天淋巴样细胞(ILCs)和CD4 T细胞的特化的一个核心的、尚未解决的问题。自从ILC亚群的发现和它们与T细胞亚群的功能平行以来,人们一直不清楚每种免疫细胞群的独特功能是什么。”
该研究使用了由Citrobacter rodentium引起的结肠细菌感染的小鼠,该小鼠模拟了由肠致病性和肠出血性大肠杆菌引起的人类疾病。老鼠和人类的结肠都有表面肠上皮细胞或表面iec,它们面向结肠腔,排列在结肠隐窝口。结肠隐窝是结肠中无数微小的凹痕,形状像厚壁试管;每个地窖的底部都有干细胞产生了所有新的IEC子集。
每个隐窝大约只有75到110个细胞深,周长只有23个细胞,人类结肠大约有9,950,000个隐窝。每个地窖都有iec。
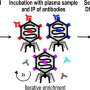
白细胞介素-22,或称IL-22,是一种细胞因子信号蛋白,由细胞产生,启动免疫反应。UAB的研究人员开发了在IL-22中具有报告基因的小鼠,因此他们可以分辨出哪些细胞产生IL-22。他们还能够针对不同的免疫细胞群缺乏IL-22,以了解细胞亚群中IL-22生产的损失对C. rodentium感染进展的影响。
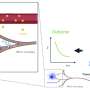
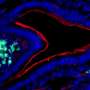
研究人员发现,在任何感染之前,先天免疫细胞的ILC3亚群是稳定状态下的主要il -22阳性细胞。在C. rodentium感染早期,第3 ~ 6天,ILC3s产生最多的IL-22。在感染后期,即第7至14天,T细胞数量增加了50倍,成为主要的IL-22生产者。此外,这两种类型的细胞有不同的微观解剖生态位——ilc3s被限制在小的、孤立的淋巴滤泡中,与隐窝有一定距离,并且在感染期间它们的数量没有增加。快速生长的T细胞包围隐窝,与ilc3相比,更接近IECs。
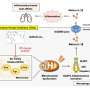
通过在两种或其中一种免疫细胞中抑制IL-22的产生,研究人员可以辨别出它们的特殊作用——既可以通过使用C. rodentium生物发光菌株观察活体小鼠的感染情况,也可以通过观察哪些IECs被IL-22激活。
在免疫系统完好的小鼠中,第3至7天,结肠中出现了一些C. rodentium生长;但是老鼠在感染中存活了下来。在ILC3s和T细胞都没有产生IL-22的小鼠中,在第3 - 7天观察到严重的C. rodentium感染,此后所有小鼠都死于感染。
ILC3s没有产生IL-22,但T细胞中仍保持IL-22生产的小鼠开始像全部IL-22敲除小鼠一样迅速屈服于感染;但40%的人存活了下来,可能是后来T细胞产生IL-22拯救了他们。只在T细胞中失去IL-22生产的小鼠比其他两种小鼠株开始晚于感染,它们显示出60%的存活率。
怀亚特和苏珊哈斯克尔病理学医学卓越主席韦弗说:“这些数据证实,先天细胞来源的IL-22在感染的早期阶段限制啮齿杆菌的定植,但在细菌抑制和宿主保护方面无法补偿T细胞来源的IL-22。”
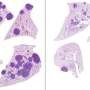
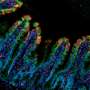
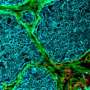
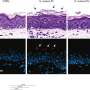
结肠切片的显微镜检查显示,免疫系统完整的小鼠在第4 - 9天的IECs表面有细菌附着,但隐窝内没有细菌生长。在所有免疫细胞或仅由T细胞产生IL-22的小鼠中,隐窝管腔内出现严重感染,到第9天,C. rodentium附着在隐窝IECs上。
当免疫细胞产生的IL-22与IECs结合时,它激活了细胞中的STAT3信号通路靶细胞从而激活或抑制靶细胞中的特定基因。
对结肠切片进行STAT3激活染色的显微镜检查显示,尽管ILC3s在抑制肠道病原菌感染早期过程中的细菌定植方面发挥了关键作用,但它们仅诱导微弱的STAT3信号,且信号仅局限于表面iec。相反,当感染进展时,T细胞通过向隐窝IECs和表面IECs传递IL-22来促进结肠屏障防御,在两个IEC群体中诱导强大的、持续的STAT3信号。Zindl说:“我们的数据确定,在C. rodentium感染期间,'特化' T细胞免疫是保护结肠隐窝所必需的。”“这可能反映了T细胞的能力,不像ILC3s,迁移到隐窝上皮,并通过肽- mhc和/或表面粘附分子相互作用直接接触IECs。”
Zindl是UAB科学家I,也是这项研究的首席研究员。
由此导致的IECs基因表达变化包括用于抗菌肽的信使rna、中性粒细胞招募趋化因子和改变结肠杯状细胞和肠细胞产生的保护性粘蛋白的酶的表达升高。所有这些都有助于对抗细菌感染。相反,干扰素γ诱导的促炎基因被抑制。“这些数据揭示了T细胞衍生的IL-22的双重作用,”Zindl说,“既促进隐窝的抗菌防御,又限制不受控制的IEC和免疫细胞激活引起的组织损伤。”
“我们的研究结果表明,ILCs和T细胞在IL-22的产生和作用方面存在时空差异感染韦弗说,“它们揭示了产生il -22的T细胞在保护肠隐窝方面的不可或缺的作用。”
更多信息:Carlene L. Zindl等人,T细胞来源的白细胞介素22在结肠隐窝抗菌防御中的非冗余作用,免疫力(2022)。DOI: 10.1016 / j.immuni.2022.02.003