运动如何对抗糖尿病损害的新证据

科学家报告说,锻炼可以对抗糖尿病损害的一种方法是激活一个自然系统,当现有的血管被这种疾病破坏时,我们必须长出新的血管。
乔治亚医学院血管生物学中心的专家说,血管生成是形成新血管的能力,糖尿病不仅损害现有的血管,还阻碍了这种在疾病和损伤面前生长新血管的先天能力。
内皮细胞我们的血管是必不可少的新血管生长。
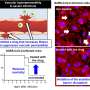
现在,MCG的科学家们有了第一个证据,在糖尿病面前,即使是一次45分钟的中等强度运动,也能使更多的外泌体(充满生物活性物质的亚微观包裹)直接向这些细胞输送更多的蛋白质ATP7A,这可以使血管生成运动,他们在报告中报告说FASEB期刊.
MCG血管生物学家和心脏病学家Tohru Fukai博士说,与我们都依赖的最复杂和最有效的递送服务不同,特别是在大流行期间,外泌体携带的物质取决于它们来自哪里和前往哪里。
虽然他和共同通讯作者MCG血管生物学家Masuko Ushio-Fukai博士还不确定这些有用的外泌体的起源,但很明显,它们传递的一个地方是内皮细胞Fukai说。
在2型糖尿病动物模型和少数50多岁的健康人群中,两周的老鼠志愿者轮跑和一次有氧运动都增加了附着在内皮细胞上的外泌体中ATP7A的水平。
科学家们指出,在这一点上,这种活动对小鼠的体重没有显著影响,但它也增加了内皮功能的标志,以及一些因素,血管内皮生长因子这是血管生成所必需的。
Ushio-Fukai说,运动也增加了强大的天然抗氧化剂细胞外超氧化物歧化酶(SOD3)的数量,但ATP7A的载荷更重,它也被认为是将必需的矿物质铜输送到细胞,这是充分利用存在的SOD3的关键。
SOD3,是一种重要的天然抗氧化剂血管平滑肌细胞在墙上血管以及骨骼肌细胞,这有助于我们保持健康的活性氧(ROS)水平。ROS是我们使用氧气的自然副产物,是一种重要的细胞信号,能够实现各种功能。但在糖尿病中,高血糖水平会导致高ROS水平,从而阻碍重要的正常功能。
福凯夫妇已经证明,糖尿病患者的ATP7A水平会降低。他们现在也有一些初步的证据表明,当将2型糖尿病久坐动物模型的血浆中循环的外泌体放在与人类内皮细胞一起的培养皿中,以及在伤口愈合的动物模型中,外泌体实际上会损害血管生成。
科学家们认为,人工合成的外泌体已经在作为药物传递机制进行研究,有朝一日可以作为“运动模拟物”来提高患者的生长能力新生血管当糖尿病损害了他们的先天能力。
事实上,他们已经生成了SOD3过表达的外泌体,并在糖尿病小鼠模型中发现了改善的血管生成和愈合。
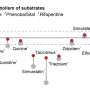
Ushio-Fukai指出,它的工作方式是,SOD3在内皮细胞中自然沉默,所以它们必须从其他细胞中获取它,因此它的重要性外来体交付。Fukai说,SOD3必须在被称为肝素结合域的自然位点与内皮细胞结合,并且铜转运蛋白ATP7A必须存在,以使SOD3在那里活跃。Fukai指出,ATP7A和结合位点都是关键。例如,当他们移除结合位点从内皮细胞中,这在自然界中是可能发生的,好处就失去了。
一旦出现并活跃,SOD3将ROS超氧化物转化为过氧化氢或H2O2,这是另一种有助于支持正常内皮细胞功能的ROS信号。Fukais报道了在人类内皮细胞中,过表达SOD3通过增加H2O2促进血管生成。
铜的连接也贯穿整个过程,因为内皮细胞经常使用大量的铜,而ATP7A,已知用于运输我们在坚果和全谷物等食物中摄入的必需矿物质,依赖于铜本身。
体育锻炼,比如跑步或在跑步机上行走,会促使肌肉收缩,从而促使外泌体释放到血液中。
当Fukai是埃默里大学心脏病科的博士后时,他是第一个证明运动增加SOD3活性的研究小组的成员。SOD3水平随着年龄的增长以及糖尿病和高血压等疾病的出现而下降。
外泌体被研究为癌症和糖尿病等多种疾病的生物标志物,以及精确的治疗传递工具。例如,由癌细胞产生的外泌体会直接磨回癌细胞。
大约十分之一的美国人有糖尿病美国疾病控制与预防中心说。
更多信息:运动改善2型糖尿病循环外泌体血管生成功能:外泌体SOD3的作用FASEB期刊(2022)。