棕榈酰化,一个新的抗癌药物的目标
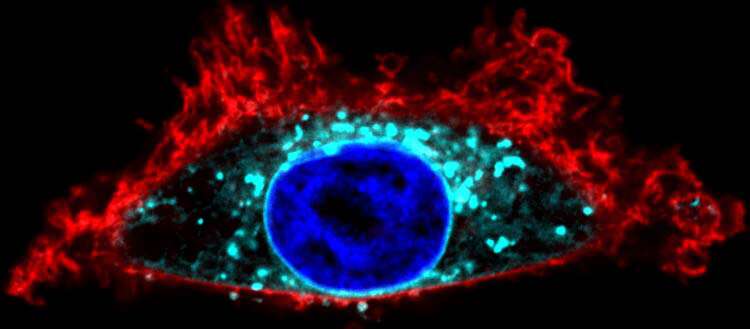
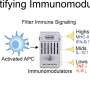
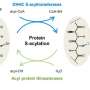
外围暂时膜蛋白与细胞膜结合,一个必要步骤能够满足他们的生物功能。要做到这一点,某些酶,催化脂质修饰来采取行动。这个过程称为棕榈酰化。这些蛋白质变异,成为致癌,如RAS蛋白,负责约三分之一的癌症。
为了理解棕榈酰化的工作方式,用它来治疗目的,日内瓦大学的科学家们(UNIGE),瑞士,开发了一种新的工具来可视化这一过程在生活细胞。他们已经表明,与被认为的相反,在高尔基体棕榈酰化不仅是可能的,通常的网站对蛋白质加工和交付,而且地方蛋白质必须采取行动,如等离子体膜。这一发现发表在《华尔街日报》自然通讯铺平了道路,创新药物研发策略目标精确膜绑定和因此活动致癌蛋白。
棕榈酰化由脂肪酸引入特定的蛋白质的他们能够绑定到细胞膜。这种机制是由精确的规则,这取决于每种类型的蛋白质的序列,以及专门的酶的存在。直到现在,科学界相信棕榈酰化的外周膜蛋白只能发生在一个地方的细胞,高尔基体。
“事实上,这些蛋白质在cytosol-the细胞生产流体和“游泳”,高尔基体,他们在哪里修改被运送之前,他们需要采取行动,“冈萨洛索利斯解释说,研究人员在细胞生理和代谢UNIGE医学院,和作者的工作。“不过,我们假设当地棕榈酰化的可能性,而不通过高尔基体。如果这是真的,它打开了全新的干预机制的可能性。”
观察和操纵蛋白质
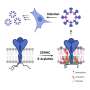
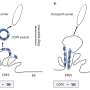
为了测试这个假说,领导的研究小组弗拉基米尔•Katanaev教授的细胞生理和代谢和转化研究中心在Onco-Hematology UNIGE医学院,专注于一种叫做Gαo的蛋白质,通常位于质膜和高尔基体。
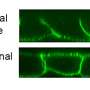
使用的方法是全新的:“我们把palmitoylating酶在细胞完全不同的隔间,核膜,”冈萨洛索利斯解释说。“Gαo招募核膜,允许我们识别特定的酶,这种酶palmitoylates他们。我们因此证实,这个过程可以发生在网站所需的蛋白质。”
与通常的生化方法相反,弗拉基米尔•Katanaev和他的团队开发的工具,他们叫SwissKASH,也是第一次来保持细胞存活和允许动态过程的观察。“直到现在,没有替代破坏细胞,“弗拉基米尔Katanaev说。“我们的方法还可以确定哪些蛋白质反应的酶,这是至关重要的,如果我们想控制机制的治疗目的。”
一种新药的目标
几个外围膜蛋白,特别是Gα和RAS蛋白亚基蛋白质,容易突变,从而获得积极的致癌潜力。他们致肿瘤性取决于它们绑定到等离子体的能力膜;棕榈酰化起着关键的作用在一个健康的细胞转变成癌。
“抑制酶诱发棕榈酰化,阻止致癌蛋白绑定的等离子体膜,可能因此化解其致病性,”冈萨洛索利斯说。“我们可以想象阻塞这个特定的反应没有整个系统失去平衡。”The scientists will now aim at automatizing this methodology to study the effect of a whole series of pharmaceutical products on the palmitoylation of selected oncoproteins, as well as testing their toxicity on the whole cell.
更多信息:冈萨洛·索利斯等地方和substrate-specific S-palmitoylation Gαo决定了亚细胞定位,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 29685 - 8