一种精细的微生物“指纹”方法跟踪单个肠道微生物菌株的变体
Casey D. Morrow博士和他在伯明翰阿拉巴马大学的同事们之前开发了一种称为WSS的微生物组“指纹”方法,通过分析粪便样本的宏基因组学数据来识别特定肠道细菌的单个菌株。他们已经证明,除非受到抗生素或减肥手术等事件的干扰,成年人体内的特定菌株往往会随着时间的推移保持稳定。他们还发现,用于治疗耐药性艰难梭菌感染的供体粪便移植菌株在移植后长达两年仍在受者体内存在。
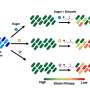
Morrow和Hyunmin Koo博士改进了指纹方法,包括在特定菌株的KEGG代谢途径中寻找单核苷酸变异。这些变异可以识别由WSS识别的单个菌株的亚菌株。例如,为了观察普通拟杆菌菌株的亚菌株,Morrow和Koo检查了该细菌中存在的23种不同的KEGG代谢途径。
他们现在已经将这种放大分析应用于监测两种关键肠道细菌b的亚菌株在较短时间内(几天或几周)的变化。普通杆菌和均匀拟杆菌。通过比较少数健康个体和住院的COVID-19患者,他们发现了亚菌株动态的差异,他们说这预示着患者内部菌株变异率的放缓。这种减缓最终可能导致微生物菌株群落的生态失调,这可能预示着肠道微生物群的优势菌株的转变。
这两种拟杆菌属在美国都有很高的丰度肠道菌群它们可能是关键物种,有助于定义整个生态系统的生物。
Koo和Morrow的研究“某些健康人类和住院COVID - 19患者的人类胃肠道微生物群落中微生物菌株失调的早期指标”发表在该杂志上科学报告.
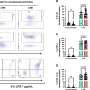
Koo和Morrow首先分析了先前发表的宏基因组学数据,这些数据来自间隔一年采样的41个人和间隔90天采样的11个人。他们在两个时间点观察了每个个体中普通芽孢杆菌的单一优势菌株,以查看它们是否表现出不同的KEGG代谢亚菌株模式,这是通过分析KEGG代谢途径中的单核苷酸变体(PKS)检测到的。总的来说,在每个个体的两个时间点之间,大多数表现出不同的亚品系PKS模式。
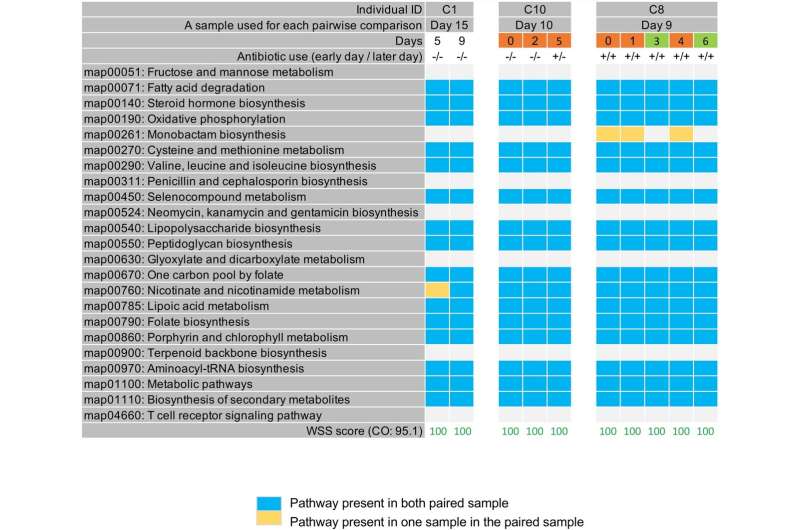
然后,UAB的研究人员分析了先前发表的宏基因组学数据,这些数据来自6名健康个体,每隔几天采样3到10周,再次通过23个KEGG中的单核苷酸变体分析亚菌株代谢途径.3个个体在每个时间点表现出不同的亚株,3个个体表现出在不同时间点出现、消失和重新出现的PKS模式。
在三名多次采样的住院COVID-19患者中,有两名患者也发现了共享的PKS模式。
Koo说:“我们认为,在压力下的肠道微生物群落,比如在COVID-19住院患者身上发现的微生物群落,可能处于一种表明优势菌株将被次要菌株击败的潜在转变状态。”“由菌株变异引起的肠道微生物群落的破坏可能反过来改变群落结构,影响代谢和定植抗性的功能。”
“综合体的特征之一生物系统当它接近一个关键的转变时,内在变化的速度会减慢,”莫罗说。“系统进入了一个与自相关相关的条件,其中模式将在时间点之间重复。共享的KEGG代谢途径簇可能代表肠道微生物菌株群落中的自相关状态,这预示着菌株的变化。”