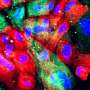
肝细胞癌中脂质组异常堆积
中科院大连化学物理研究所(DICP)朴海龙教授领导的研究小组发现了去泛素酶泛素特异性蛋白酶22 (USP22)与肝细胞癌(HCC)中脂质组异常积聚的相关性。
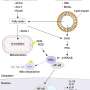
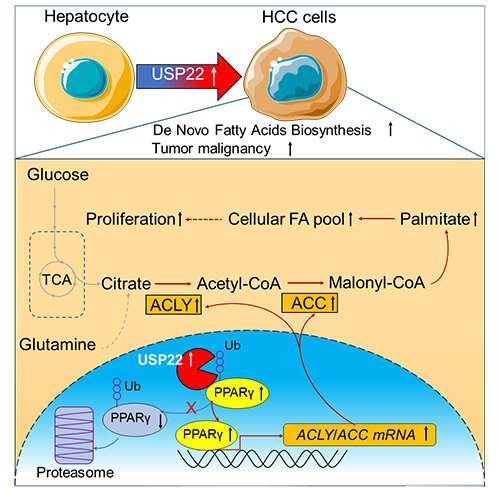
他们阐明了USP22调节的脂肪生成机制,该机制涉及过氧化物酶体增殖物激活受体γ (PPARγ) -ATP柠檬酸裂解酶(ACLY) /乙酰辅酶a羧化酶(ACC)轴在HCC肿瘤发生中的作用,并为通过USP22抑制靶向脂肪生成的治疗提供了基础。
这项研究发表在自然通讯4月21日。DICP的徐国旺教授和大连医科大学第一附属医院的谭光教授也参与了这项研究。
代谢重编程是癌症的标志之一,其中异常增加的新生脂肪生成(DNL)是最常见的特征之一。
脂肪酸在非分裂细胞中合成的速度较低,主要是从细胞外循环中吸收脂类。相反,DNL,尤其是从头开始脂肪酸合成,是一个重要的脂质来源癌症细胞.
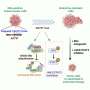
在本研究中,研究人员通过免疫印迹法检测了USP家族成员在HCC组织中的表达,并与配对的正常相邻组织进行了比较。他们进一步筛选了不同的代谢物液相色谱法质谱分析。
结果表明,USP22是USP中最显著的高表达成员,且USP22的高表达与脂质及类脂代谢产物的上调有关。
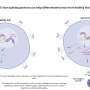
分子生化实验证实USP22有调节作用脂质代谢PPARγ是一种配体激活的转录因子,属于核激素受体家族,通过上调ACC、ACLY和脂肪酸合成酶(FASN)等脂质合成酶来促进脂肪生成。
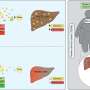
PPARγ是USP22的底物,USP22介导的去泛素化稳定了PPARγ并激活了PPARγ靶基因(即ACC和ACLY),有助于脂肪生成和HCC肿瘤的发生。
朴教授说:“这项研究提供了一种针对脂肪酸合成的选择,这可能有利于HCC中USP22高表达的患者。”
更多信息:宁贞等,USP22通过稳定PPARγ在肝细胞癌中调控脂质组积累,自然通讯(2022)。DOI: 10.1038 / s41467 - 022 - 29846 - 9