新的基于crispr的图谱将每个人类基因与其功能联系在一起

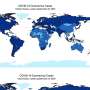
人类基因组计划(Human Genome Project)是一项雄心勃勃的计划,旨在对人类的每一个DNA片段进行测序。该项目吸引了来自世界各地研究机构的合作者,包括麻省理工学院的怀特黑德生物医学研究所,最终于2003年完成。bob88体育平台登录现在,20多年过去了,麻省理工学院教授乔纳森·韦斯曼(Jonathan Weissman)和他的同事们已经超越了这一序列,首次展示了人类细胞中表达的基因的全面功能图。该项目的数据于6月9日在网上公布细胞该方法将每个基因与其在细胞中的工作联系在一起,是单细胞测序方法Perturb-seq多年合作的结晶。
数据如下可供其他科学家使用。“这是一种很大的资源人类基因组是一个很大的资源,因为你可以进入并进行基于发现的研究,”韦斯曼说,他也是怀特海研究所的成员,也是霍华德休斯医学研究所的研究员。“你不需要提前定义你要研究的生物学,而是有了基因型-表型关系的地图,你可以在不做任何实验的情况下进入并筛选数据库。”
该屏幕使研究人员能够深入研究各种各样的生物学问题。他们用它来探索功能未知的基因对细胞的影响,研究线粒体对压力的反应,以及筛选导致染色体丢失或增加的基因,这种表型在过去已被证明很难研究。“我认为这个数据集将使各种各样的分析成为可能,我们甚至还没有想到来自生物学其他领域的人,突然他们就有了可用的数据,”前韦斯曼实验室博士后汤姆·诺曼说,他是该论文的共同高级作者。
先锋Perturb-seq
该项目利用了Perturb-seq方法,可以以前所未有的深度跟踪打开或关闭基因的影响。这个方法是2016年首次发布由包括韦斯曼和麻省理工学院教授阿维夫·雷格夫在内的一组研究人员完成,但只能用于小组基因,而且成本很高。
庞大的扰动-seq地图是由Joseph Replogle博士的基础工作实现的。韦斯曼实验室的学生,本论文的共同第一作者。诺曼现在领导着纪念斯隆·凯特琳癌症中心的一个实验室。普林斯顿大学分子生物学系助理教授Britt Adamson;以及10x Genomics的一个团队,着手创建一个可以扩大规模的新版本的Perturb-seq。研究人员发表了一份概念验证论文在自然生物技术在2020年。
Perturb-seq方法使用CRISPR-Cas9基因组编辑将遗传变化引入细胞,然后使用单细胞RNA测序来捕获由给定遗传变化引起的表达的RNA的信息。由于rna控制着细胞行为的各个方面,这种方法可以帮助解码基因变化对细胞的许多影响。
自从Weissman、Regev和其他人发表了最初的概念验证论文以来,他们已经在更小的范围内使用了这种测序方法。例如,研究人员在2021年使用Perturb-seq来探索人类和病毒基因在感染HCMV(一种常见的疱疹病毒)过程中如何相互作用。
在这项新研究中,Replogle和合作者,包括Weissman实验室的研究生、论文的共同第一作者Reuben Saunders,将这种方法扩展到整个基因组。利用人类血液癌细胞系以及来自视网膜的非癌细胞,他对超过250万个细胞进行了Perturb-seq,并利用这些数据建立了一个将基因型与表型联系起来的综合地图。
深入研究数据
在完成筛选后,研究人员决定将他们的新数据集用于研究一些生物学问题。“Perturb-seq的优势在于,它可以让你以一种公正的方式获得一个大数据集,”汤姆·诺曼(Tom Norman)说。“没有人完全知道你能从这种数据集中得到什么。现在的问题是,你要用它来做什么?”
第一个,也是最明显的应用是研究功能未知的基因。由于该筛查也读出了许多已知基因的表型,研究人员可以利用这些数据将未知基因与已知基因进行比较,并寻找相似的转录结果,这可能表明基因产物作为更大复合体的一部分共同工作。
一种名为C7orf26的基因突变尤其引人注目。研究人员注意到,那些被去除导致类似表型的基因是一种称为积分器的蛋白质复合体的一部分,这种蛋白质复合体在制造小核rna中起着作用。积分器复合体由许多更小的亚基组成——以前的研究表明有14个单独的蛋白质——研究人员能够证实C7orf26构成了复合体的第15个组成部分。
他们还发现,15个子单元在更小的模块中一起工作,在集成器复合体中执行特定的功能。桑德斯说:“如果没有这种一千英尺高的视角,就不清楚这些不同的模块在功能上是如此不同。”
Perturb-seq的另一个好处是,由于检测重点是单个细胞,研究人员可以使用这些数据来观察更复杂的表型,当它们与其他细胞的数据一起研究时,这些表型就会变得混乱。韦斯曼说:“我们经常把所有‘X基因’被敲除的细胞放在一起,并对它们进行平均,以观察它们是如何变化的。”“但有时,当你敲除一个基因时,失去同一基因的不同细胞表现不同,而这种行为可能会被平均水平所忽略。”
研究人员发现,导致细胞间不同结果的一个基因子集是染色体分离的原因。它们的去除会导致细胞失去一条染色体或多出一条染色体,这种情况被称为非整倍体。魏斯曼说:“你无法预测失去这个基因后的转录反应是什么,因为它取决于你获得或失去哪条染色体的次要效应。”“我们意识到,我们可以扭转这一局面,创造出这种复合表型,寻找染色体获得和丢失的特征。通过这种方式,我们对正确分离DNA所需的因素进行了第一次全基因组筛选。”
诺曼说:“我认为非整倍体研究是迄今为止这些数据最有趣的应用。”“它捕获了一种只能使用单细胞读数获得的表型。你不能用其他方式去追求它。”
研究人员还利用他们的数据集研究了线粒体对压力的反应。线粒体由自由生活的细菌进化而来,在它们的基因组中携带13个基因。在核DNA中,大约有1000个基因以某种方式与线粒体功能有关。“长期以来,人们一直对细胞核DNA和线粒体DNA在不同细胞条件下如何协调和调节感兴趣,特别是当细胞受到压力时,”Replogle说。
研究人员发现,当他们扰动不同的线粒体相关基因在美国,核基因组对许多不同的基因变化做出了类似的反应。然而,线粒体基因组的反应变化更大。
“为什么线粒体仍然有自己的DNA,这仍然是一个悬而未决的问题,”Replogle说。“从我们的工作中得出的一个大结论是,拥有一个单独的线粒体基因组的一个好处可能是,在应对不同的压力源时,有局部的或非常特定的基因调控。”
“如果你有一个线粒体坏了,另一个以不同的方式坏了,这些线粒体可能会有不同的反应,”韦斯曼说。
在未来,研究人员希望将Perturb-seq用于不同类型的细胞除了癌细胞之外。他们还希望继续探索他们的基因功能图谱,并希望其他人也能这样做。诺曼说:“这确实是作者和其他合作者多年工作的顶峰,我很高兴看到它继续成功和扩展。”