慢性疼痛相关基因的发现创造了新的治疗靶点
牛津大学的研究人员发现了一种基因,可以通过放大脊髓内的疼痛信号来调节疼痛致敏,帮助他们理解人类慢性疼痛的一个重要机制,并提供了一个新的治疗靶点。
慢性疼痛是一个普遍的问题,影响着全球数百万人,但为什么有些人更容易得它,以及什么因素导致慢性疼痛没有被完全理解。
众所周知,反复的刺激,比如用锋利的针刺,会导致对疼痛的敏感度增强。这个过程被称为“疼痛闭合”,并导致临床疼痛障碍。
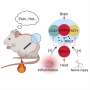
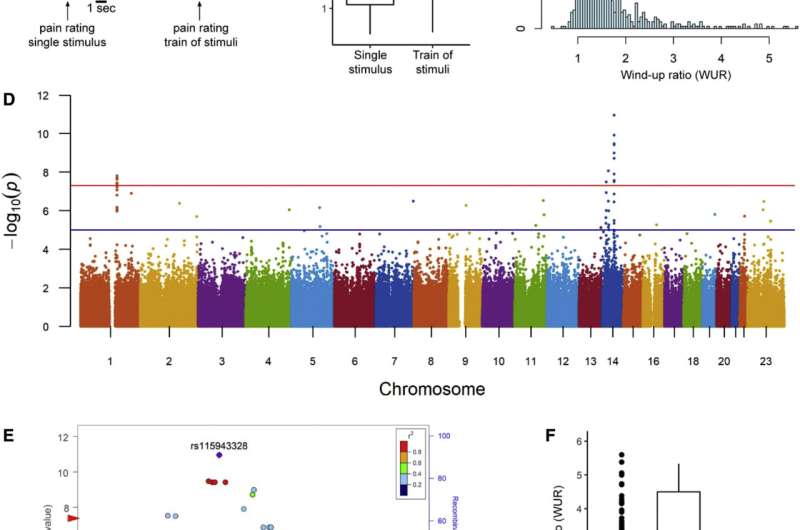
在一项分两部分的研究中,牛津大学纳菲尔德临床神经科学系的研究人员首先进行了比较遗传变异对来自哥伦比亚的1000多名参与者的样本进行了分析,以寻找在经历更大疼痛的人身上是否存在更常见的基因变异的线索。他们注意到一个特定基因(钠钙交换蛋白3型,NCX3)的变异有显著差异。
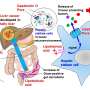
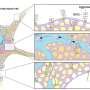
随后,研究人员在小鼠身上进行了一系列实验,以了解NCX3是如何调节疼痛闭合的,以及它是否可能是一个治疗靶点。NCX3在小鼠体内表达脊髓处理和传输的神经元疼痛信号到大脑。这些神经元需要NCX3来输出活动后积累的多余钙。在NCX3缺失的情况下,脊髓神经元对外周损伤信号的反应更加活跃,疼痛闭合增加。
相反,增加脊髓内NCX3的水平可以减轻小鼠的疼痛。
纳菲尔德临床神经科学系神经学和神经生物学教授大卫·班尼特说:“这是我们第一次能够研究人类的疼痛,然后直接在老鼠身上展示疼痛背后的机制,这让我们对相关因素有了真正广泛的了解,以及我们如何开始开发新的治疗方法。”
班尼特教授补充说:“慢性疼痛是一个全球性问题,会极大地削弱人的身体。我们在哥伦比亚进行了这项研究,因为那里的人口是混合血统,包括土著印第安人、非洲人和欧洲人,这给我们提供了广泛的基因多样性来研究。这使得这些发现非常令人兴奋,因为它们具有潜在的国际应用价值。
“研究结果表明,任何可以增加NCX3活性的药物都可以降低其活性疼痛人类的致敏性。”