研究确定了新的DNA帕金森病风险的线索
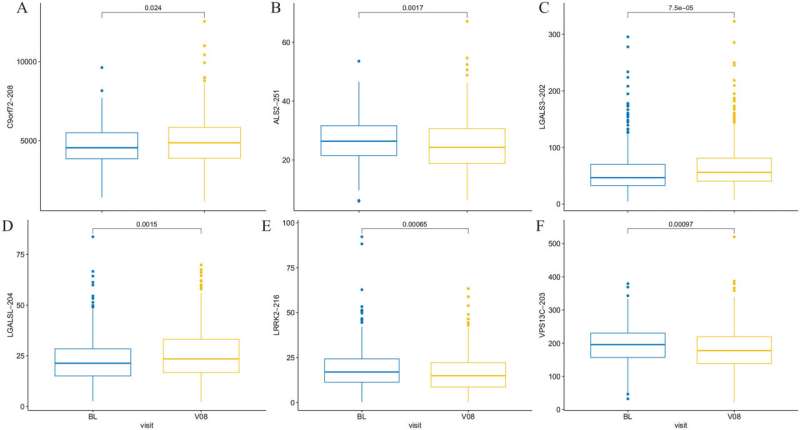
发现一个新的帕金森病研究开辟了一个激动人心的大道为开发治疗干预的发展这种常见的运动障碍。
的专题文章实验生物学和医学对理解遗传过程潜在的帕金森患者的神经细胞变性。
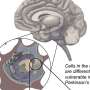
Sulev教授领导的研究中,角在澳大利亚西部的阶石神经和转化科学研究所和默多克大学报道,改变初生的转录的基因内区(有关DNA测序)可能是帕金森氏症的风险和发展指标。
“更好地了解神经细胞变性的机制可以帮助开发靶向治疗帕金森氏症患者,“灭世狂舞教授说。“多年来寻找DNA特定的疾病,如帕金森症的危险因素一直专注于外显子,我们百分之二的基因组编码的蛋白质的信息。
“大量的DNA风险驻留在其他98%的基因决定了,什么时候,多长时间生产外显子来生成这些蛋白质。
“同样,以往的研究都集中在特定的测量外显子细胞,忽略non-exon的大部分材料,可以影响他们的功能。”
阿比盖尔博士在这项研究中,角教授,普法夫(阶石研究所和默多克大学),和利物浦大学的薇薇安博士Bubb和约翰·奎因分析了内含子和调查与帕金森病相关的变化疾病进展。
研究显示内含子的重要性在调节细胞功能,导致的变化。
“我们的研究强调了内含子的重要性作为潜在调节器调节细胞功能通过操纵细胞如何使用外显子,“灭世狂舞教授说。“这项工作打开一个基因组的研究对发展中的新方法新途径改善诊断和更有针对性的治疗帕金森病的进展。”
本文题为“纵向intronic RNA-Seq帕金森症患者的分析,将揭示特定疾病的转录。”
史蒂文·古德曼博士主编实验生物学和医学说,这项研究说明了额外的blood-based生物标记与潜在风险的预测和诊断帕金森病的进展。
进一步探索