辉瑞要求FDA批准5岁以下的COVID-19疫苗
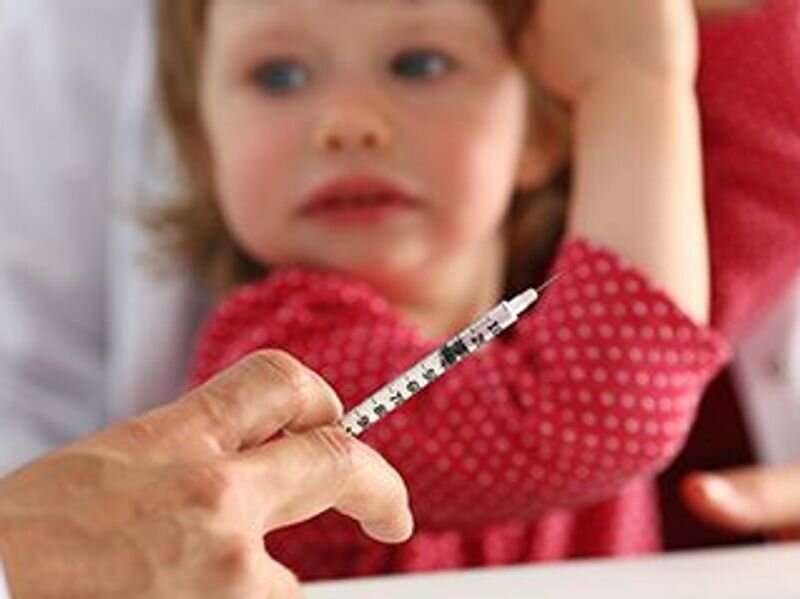
辉瑞公司(Pfizer Inc.)周三表示,已请求美国食品和药物管理局(fda)批准在5岁以下儿童中紧急使用其新冠肺炎疫苗。
该公司在一份声明中表示,已向fda提供了2/3阶段试验的数据,其中包括近1700人孩子们当欧米克隆是显性变异时,他们接种了第三剂疫苗。
试验表明,该疫苗引发了强烈的免疫反应,是安全的。该公司说,第三次注射一个月后,儿童体内的抗体水平与第二次注射后16至25岁人群的抗体水平相似。在试验中期,该疫苗在预防有症状的COVID-19方面的有效性为80.3%。的发现均于5月23日发布,但尚未经过同行评审或发表在医学杂志上。
参与试验的儿童接受了三次3微克的剂量,前两剂间隔三周给药第三个剂量至少在第二剂后两个月服用。6个月至5岁儿童的剂量小于年龄较大的群体。5至12岁的儿童接种两剂10微克的疫苗,12岁及以上的人接种两剂30微克的疫苗。两组人都有资格接受强化剂量,美国有线电视新闻网报道。
5岁以下的儿童是美国唯一没有资格接种COVID-19疫苗的年龄组。4月底,Moderna向FDA提供了在6个月至5岁儿童中使用其COVID-19疫苗的试验数据。一个由FDA疫苗专家组成的小组准备满足在这两家公司中,Moderna和辉瑞要求紧急使用COVID-19疫苗年幼的孩子.
©2022每日健康.版权所有。